Aandeelhouders niet bevoegd op te treden
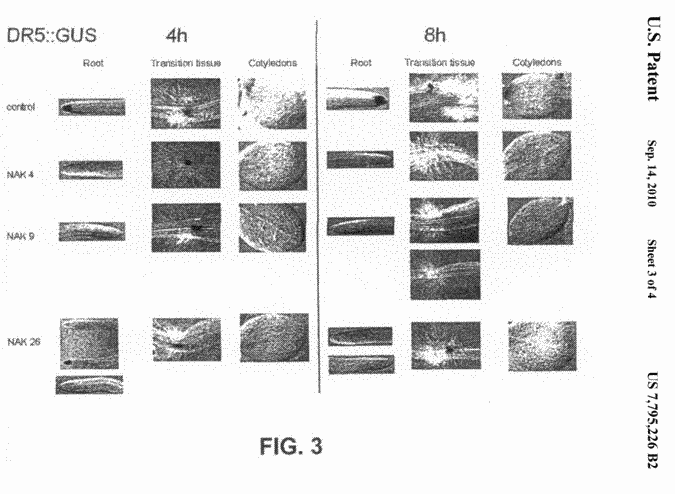 Octrooirecht. Stukgelopen samenwerking. Financiering van onderzoek, behandeling van groot aantal (ernstige) ziekten. Geschil over de constructie rondom octrooibeheer. Overdracht van "patenten, vergunningen, know-how, en intellectuele en industriële eigendomsrechten" aan nog op te richten vennootschap, nu Biotempt B.V.. Vordering is afgewezen omdat slechts het bestuur bevoegd is octrooirechtelijke vorderingen in te stellen en niet aandeelhouders. Ook onrechtmatig handelen afgewezen, nader onderbouwing behoeft volgens de rechtbank niet gezien de talloze stukken en de uitgebreide behandeling.
Octrooirecht. Stukgelopen samenwerking. Financiering van onderzoek, behandeling van groot aantal (ernstige) ziekten. Geschil over de constructie rondom octrooibeheer. Overdracht van "patenten, vergunningen, know-how, en intellectuele en industriële eigendomsrechten" aan nog op te richten vennootschap, nu Biotempt B.V.. Vordering is afgewezen omdat slechts het bestuur bevoegd is octrooirechtelijke vorderingen in te stellen en niet aandeelhouders. Ook onrechtmatig handelen afgewezen, nader onderbouwing behoeft volgens de rechtbank niet gezien de talloze stukken en de uitgebreide behandeling.
4.9. de vorderingen onder 3.1.4.c. en 3.1.4.d. die neerkomen op een verbod aan EAS om inbreuk te maken op de aan Biotempt toebehorende patenten en om gebruik te maken van de aan Biotempt toebehorende technologie en know how.
4.9.a. [B] c.s. legt aan deze vorderingen het volgende ten grondslag. [C] heeft toegestaan dat EBI op basis van informatie van EAS met het radiatie octrooi en de uitvinding op het gebied van nierfalen (renal failure) aan de haal is gegaan, terwijl dit niet binnen de licentieovereenkomst valt. EAS en EBI maken met hun onderzoek en hun publiciteit op internet inbreuk op de door Biotempt gehouden octrooien. [C] dient als bestuurder van Biotempt op te treden tegen deze inbreuk. De op de octrooien inbreuk makende activiteiten van EBI op basis van informatie van EAS brengen schade toe aan Biotempt, zodat [B] c.s. als aandeelhouder van Biotempt belang heeft bij het gevorderde verbod.
4.9.b. Het is aan het bestuur van Biotempt en niet aan [B] c.s. als aandeelhouder van Biotempt om dergelijke vorderingen in te stellen. Die vorderingen zullen daarom worden afgewezen.
4.10. de vordering onder 3.1.5. te verklaren voor recht dat [C], Zist, Expolin en/of EAS onrechtmatig hebben gehandeld
Uit de beoordeling van alle hiervoor besproken vorderingen van [B] c.s. volgt dat van onrechtmatig handelen van [C], Zist, Expolin en EAS niet is gebleken. Gezien de talloze stukken en de uitgebreide behandeling in deze zaak gaat het ook verder niet aan om zonder enige nadere onderbouwing, die ontbreekt, [C], Zist, Expolin en/of EAS onrechtmatig handelen te verwijten. Deze vordering zal dan ook als te vaag en te algemeen worden afgewezen.
Lees het vonnis hier.
 Verdachte heeft een afslankinstituut geëxploiteerd, waar werd gewerkt met de zogenaamde dr. Simeonstherapie. Deze therapie combineert een laag calorisch dieet (500 calorieën) met het gebruik van het geneesmiddel hCG. hCG is het werkzame bestanddeel van het receptgeneesmiddel Pregnyl, dat in Nederland is geregistreerd voor onvruchtbaarheidsbehandelingen. hCG wordt gewonnen uit de urine van zwangere vrouwen en is bekend van de publieksactie "Moeders voor Moeders" Vergelijk met (
Verdachte heeft een afslankinstituut geëxploiteerd, waar werd gewerkt met de zogenaamde dr. Simeonstherapie. Deze therapie combineert een laag calorisch dieet (500 calorieën) met het gebruik van het geneesmiddel hCG. hCG is het werkzame bestanddeel van het receptgeneesmiddel Pregnyl, dat in Nederland is geregistreerd voor onvruchtbaarheidsbehandelingen. hCG wordt gewonnen uit de urine van zwangere vrouwen en is bekend van de publieksactie "Moeders voor Moeders" Vergelijk met ( Strafrecht. Verdachte, een gepensioneerd huisarts, heeft zijn medewerking verleend aan een afslankinstituut, waar werd gewerkt met de zogenaamde dr. Simeonstherapie. Deze therapie combineert een laag calorisch dieet (500 calorieën) met het gebruik van het geneesmiddel hCG. hCG is het werkzame bestanddeel van het receptgeneesmiddel Pregnyl, dat in Nederland is geregistreerd voor onvruchtbaarheidsbehandelingen. hCG wordt gewonnen uit de urine van zwangere vrouwen en is bekend van de publieksactie "Moeders voor Moeders". In het afslankinstituut werd het geneesmiddel gebruikt om het hongergevoel te onderdrukken. Verdachtes medeverdachten bereidden zelf injectiespuiten met hCG en gaven deze spuiten mee aan klanten. Verdachte verleende hieraan onder meer zijn medewerking door de recepten voor het geneesmiddel Pregnyl uit te schrijven. Door aldus te handelen hebben de verdachten de Geneesmiddelenwet overtreden, die geschreven is om de volksgezondheid te beschermen.
Strafrecht. Verdachte, een gepensioneerd huisarts, heeft zijn medewerking verleend aan een afslankinstituut, waar werd gewerkt met de zogenaamde dr. Simeonstherapie. Deze therapie combineert een laag calorisch dieet (500 calorieën) met het gebruik van het geneesmiddel hCG. hCG is het werkzame bestanddeel van het receptgeneesmiddel Pregnyl, dat in Nederland is geregistreerd voor onvruchtbaarheidsbehandelingen. hCG wordt gewonnen uit de urine van zwangere vrouwen en is bekend van de publieksactie "Moeders voor Moeders". In het afslankinstituut werd het geneesmiddel gebruikt om het hongergevoel te onderdrukken. Verdachtes medeverdachten bereidden zelf injectiespuiten met hCG en gaven deze spuiten mee aan klanten. Verdachte verleende hieraan onder meer zijn medewerking door de recepten voor het geneesmiddel Pregnyl uit te schrijven. Door aldus te handelen hebben de verdachten de Geneesmiddelenwet overtreden, die geschreven is om de volksgezondheid te beschermen.
 Wet geneesmiddelenprijzen. Regeling referentieprijslijsten geneesmiddelen (RRG). De minister heeft niet in strijd met artikel 1, aanhef en onder a, van de RRG de Tvz-lijst buiten beschouwing mogen laten bij het vaststellen van de maximumprijs van de geneesmiddelen.
Wet geneesmiddelenprijzen. Regeling referentieprijslijsten geneesmiddelen (RRG). De minister heeft niet in strijd met artikel 1, aanhef en onder a, van de RRG de Tvz-lijst buiten beschouwing mogen laten bij het vaststellen van de maximumprijs van de geneesmiddelen. In navolging van
In navolging van  Bijzondere overeenkomsten. Geneeskundige behandelingsovereenkomst. Inbrengen anticonceptiemiddel. Procesrecht. Ingevolge art. 130 lid 2 Rv geen hogere voorziening tegen het, op een aan de feitenrechter voorbehouden uitleg van de gedingstukken gebaseerde, oordeel dat eisvermeerdering in strijd is met de eisen van een goede procesorde.
Bijzondere overeenkomsten. Geneeskundige behandelingsovereenkomst. Inbrengen anticonceptiemiddel. Procesrecht. Ingevolge art. 130 lid 2 Rv geen hogere voorziening tegen het, op een aan de feitenrechter voorbehouden uitleg van de gedingstukken gebaseerde, oordeel dat eisvermeerdering in strijd is met de eisen van een goede procesorde. Geneesmiddel. Maximumprijs. Bij besluit van 19 februari 2009 heeft de minister de bijlage bij de
Geneesmiddel. Maximumprijs. Bij besluit van 19 februari 2009 heeft de minister de bijlage bij de 

















