Overeenkomst van opdracht met Friquez rechtsgeldig opgezegd door Novaclin
Ktr. Rechtbank Amsterdam 11 februari 2014, ECLI:NL:RBAMS:2014:1374 (Friquez tegen Novaclin) Overeenkomst van opdracht. Novaclin houdt zich bezig met de ontwikkeling en verhandeling van medicijnen en andere hulpmiddelen op de internationale markt. Eindvonnis waarin wordt beoordeeld of de tussen partijen gesloten overeenkomst van opdracht rechtsgeldig is opgezegd. Daarbij dient de vraag te worden beantwoord of partijen een regeling met betrekking tot de tussentijdse opzegging van de overeenkomst zijn overeengekomen. Het verweer van gedaagde dat de overeenkomst met wederzijds goedvinden is beëindigd wordt verworpen. Ten overvloede overweegt de kantonrechter dat zelfs in het geval wel overeenstemming was bereikt over de tussentijdse beëindiging van de overeenkomst, eiser daaraan niet gebonden is, omdat niet kan worden aangenomen dat de aan eiser toe te rekenen schijn van bevoegdheid van de gedetacheerde is gewekt.
Overeenkomst van opdracht. Novaclin houdt zich bezig met de ontwikkeling en verhandeling van medicijnen en andere hulpmiddelen op de internationale markt. Eindvonnis waarin wordt beoordeeld of de tussen partijen gesloten overeenkomst van opdracht rechtsgeldig is opgezegd. Daarbij dient de vraag te worden beantwoord of partijen een regeling met betrekking tot de tussentijdse opzegging van de overeenkomst zijn overeengekomen. Het verweer van gedaagde dat de overeenkomst met wederzijds goedvinden is beëindigd wordt verworpen. Ten overvloede overweegt de kantonrechter dat zelfs in het geval wel overeenstemming was bereikt over de tussentijdse beëindiging van de overeenkomst, eiser daaraan niet gebonden is, omdat niet kan worden aangenomen dat de aan eiser toe te rekenen schijn van bevoegdheid van de gedetacheerde is gewekt.
3.9. Op grond van artikel 3.2. van de conceptovereenkomst had Novaclin - zoals Friquez stelt - de overeenkomst schriftelijk moeten opzeggen met inachtneming van een opzegtermijn van één maand. Novaclin heeft daartegen aangevoerd dat zij de overeenkomst in het gesprek van 17 september 2012 heeft opgezegd.
De kantonrechter is van oordeel dat de mededeling van [naam 3] aan [naam 2] in het gesprek van 17 september 2012 inhoudende dat de overeenkomst wordt beëindigd als een opzegging kan worden beschouwd, maar niet tegen de door Novaclin voorgestane datum van 1 oktober 2012. Friquez had uit de mededeling van [naam 3] en het vervolgens wegsturen van [naam 2] kunnen en moeten afleiden dat Novaclin de overeenkomst tussentijds wenste te beëindigen. In het gesprek heeft [naam 3] immers uitdrukkelijk aan [naam 2] medegedeeld dat de overeenkomst werd beëindigd. Dat deze mededeling Friquez heeft bereikt volgt uit de stelling in de dagvaarding dat [naam 2] Friquez heeft geïnformeerd dat Novaclin kennelijk over wilde gaan tot tussentijdse opzegging van de overeenkomst. Uit de onder r.o. 1.11 genoemde brief van 4 oktober 2012 van (de gemachtigde van) Friquez blijkt dat Friquez deze mededeling ook zo heeft opgevat. Immers, de gemachtigde van Friquez schrijft dat Novaclin heeft aangekondigd de samenwerking voortijdig te willen beëindigen. Novaclin heeft, mede gelet op het voorgaande, uit het handelen van Friquez mogen afleiden dat Friquez begreep dat Novaclin de overeenkomst wenste op te zeggen. Friquez heeft weliswaar na 17 september 2012 facturen verzonden, maar niet is gebleken dat [naam 2] zich beschikbaar heeft gesteld voor werk. Friquez heeft dit wel gesteld, maar niet met concrete feiten onderbouwd. Dat de opzegging niet overeenkomstig artikel 3.2. van de conceptovereenkomst schriftelijk is geschied, doet gelet op de hiervoor genoemde omstandigheden, niet af aan de rechtsgeldigheid van de opzegging. De achtergrond van een dergelijke bepaling is immers het zekerstellen van de ontvangst van de opzegging door de geadresseerde. Het staat echter niet ter discussie dat de opzegging Friquez heeft bereikt.
3.10. Het voorgaande leidt tot de conclusie dat de overeenkomst tussen Friquez en Novaclin op 17 september 2012 door Novaclin is opgezegd. Uitgaande van de overeengekomen opzegtermijn van één maand, is de overeenkomst tussen Friquez en Novaclin op 31 oktober 2012 beëindigd.
Lees de uitspraak:
ECLI:NL:RBAMS:2014:1374 (link)
ECLI:NL:RBAMS:2014:1374 (pdf)
Informatie op website van ECOstyle misleidend in de zin van Verordening gewasmiddelenbescherming
CVB 12 maart 2014, dossiernummer 2013/00803 (ECOstyle)
De beslissing van het College van Beroep
Op grond van het hierboven overwogene acht het College de informatie op de website van ECOstyle over Ultima Professioneel in strijd met artikel 2 NRC wegens het daarin ontbreken van mededelingen als voorgeschreven door artikel 66 lid 1 en lid 6 Verordening 1107/2009. Voorts acht het College de informatie op de website in strijd met artikel 2 NRC, nu sprake is van misleiding in de zin van artikel 66 lid 2 Verordening 1107/2009 voor zover het betreft de mededeling “geen beperkingen rondom rioolputten of langs open water”.
Ten aanzien van het voorgaande vernietigt het College de beslissing van de Commissie.
Voor het overige bevestigt het College de bestreden beslissing.
VGZ moet sponsorovereenkomst en overeenkomst medische dienstverlening met SSM gestand doen
 |
Contractenrecht. Partijen hebben in 2011 een sponsorovereenkomst en een overeenkomst medische dienstverlening gesloten en afgesproken dat VGZ inzake de overeenkomst medische dienstverlening ieder jaar € 200.000,00 op een rekening van SSM zou storten. SSM zou VGZ voor de tijdens evenementen verleende medische diensten declaraties sturen. Zodra VGZ haar akkoord hierop zou geven, zou SSM definitief de beschikking krijgen over de bedragen. Tevens is overeengekomen dat een model-declaratieformulier zou worden gehanteerd voor de financiële verantwoording en afwikkeling.
SSM vordert VGZ te bevelen op basis van de door haar ingediende declaraties het resterende budget voor 2013 vrij te geven. De rechtbank beveelt VGZ de beide met SSM gesloten overeenkomsten na te komen en gestand te doen.
5.14. De voorzieningenrechter is van oordeel dat tussen partijen nader overleg had moeten plaatsvinden, alvorens VGZ tot opzegging van de overeenkomsten over had mogen gaan. Dat SSM heeft stilgezeten en geen actie heeft ondernomen, zoals VGZ stelt, is onvoldoende aannemelijk geworden. SSM heeft diverse stukken overgelegd waaruit blijkt dat zij een toelichting heeft gegeven op bepaalde vraagpunten. Verder heeft er op 16 augustus 2013 een bestuursvergadering van SSM plaatsgevonden, waarna SSM VGZ toezeggingen heeft gedaan en is er naar aanleiding van de audit op 27 september 2013 een uitvoerig verslag van de accountant opgesteld waarin uitleg wordt gegeven over de BTW-vrijstelling van medische diensten. De redenen die VGZ heeft aangevoerd, rechtvaardigen, voorshands geoordeeld en mede gelet op de voorgeschiedenis tussen partijen – welke relatie overigens dateert van de jaren ’90 – , een opzegging van de beide overeenkomsten niet. Voornoemde punten zijn redenen, zoals hiervoor reeds is overwogen, voor nader overleg, althans om dit overleg nader te concretiseren, hetgeen ook geldt voor de samenwerking tussen partijen in het algemeen.
5.15. Dit betekent dat VGZ zal worden veroordeeld de beide met SSM gesloten overeenkomsten (de sponsorovereenkomst en de overeenkomst medische dienstverlening) na te komen en gestand te doen. Aan deze veroordeling zal een dwangsom worden verbonden, zoals hierna volgt.
Lees de uitspraak:
ECLI:NL:RBGEL:2013:6477 (link)
ECLI:NL:RBGEL:2013:6477 (pdf)
Verbod VGG eenzijdig doorberekenen BTW bovenop vergoeding
Vzr. Rechtbank Gelderland 23 december 2013, ECLI:NL:RBGEL:2013:6476 (Eisers tegen VGG Zorg) BTW. Voorliggende vraag is of VGG Zorg gerechtigd was om, zonder instemming van de vrijgevestigde psychotherapeuten (eisers), de btw eenzijdig door te berekenen bovenop het tarief voor de vergoeding van de kosten van dienstverlening. Voorshands geoordeeld heeft VGG Zorg daarmee gehandeld in strijd met de overeenkomst. De rechtbank oordeelt dat dat het gevorderde verbod voor VGG Zorg om over de door de vrijgevestigden behaalde omzet over 2013 btw in rekening te brengen dan wel te verrekenen, zal worden toegewezen.
BTW. Voorliggende vraag is of VGG Zorg gerechtigd was om, zonder instemming van de vrijgevestigde psychotherapeuten (eisers), de btw eenzijdig door te berekenen bovenop het tarief voor de vergoeding van de kosten van dienstverlening. Voorshands geoordeeld heeft VGG Zorg daarmee gehandeld in strijd met de overeenkomst. De rechtbank oordeelt dat dat het gevorderde verbod voor VGG Zorg om over de door de vrijgevestigden behaalde omzet over 2013 btw in rekening te brengen dan wel te verrekenen, zal worden toegewezen.
4.8. Ten aanzien van de stelling van VGG Zorg dat, als gevolg van de kostenontwikkeling van het Servicebedrijf het niet langer verantwoord was om de btw-afdrachten nog langer te dekken uit de middelen voor de dienstverlening, wordt overwogen dat het op de weg van VGG Zorg had gelegen om hierover met de vrijgevestigden in overleg te treden door eerst de vrijgevestigden op de door haar vermeende constateringen te wijzen en vervolgens de vrijgevestigden de gelegenheid te geven om hierop te reageren.
4.9. Door eenzijdig de btw-afdracht met ingang van 1 januari 2013 ten laste te brengen van de vrijgevestigden handelt VGG Zorg derhalve, voorshands geoordeeld, in strijd met de betreffende bepalingen uit de overeenkomst. Het gevorderde verbod voor VGG Zorg om over de door de vrijgevestigden behaalde omzet over 2013 btw in rekening te brengen dan wel te verrekenen, zal worden toegewezen.
Lees de uitspraak:
ECLI:NL:RBGEL:2013:6476 (link)
ECLI:NL:RBGEL:2013:6476 (pdf)
Geen vergelijkende reclame meer nu borden niet meer verwijzen naar andere medicijnen
CGR 6 maart 2014, AA14.005
In 2012 is een advertentie voor [geneesmiddel Z] onderwerp geweest van een klacht, die bij de Codecommissie is ingediend. De klacht betrof een advertentie die bestond uit een folder “[titel A]” waarin de afbeelding van een wegbewijzering was vermeld met daarop aangegeven twee routes: de [geneesmiddel Z] route die naar voren ging richting de zon en die licht werd afgebeeld en de route van de [antistoffen B] die in het donker naar achteren was geplaatst. Verzoekster heeft een nieuwe advertentie gemaakt en vraagt nu advies over de toelaatbaarheid van deze advertentie. De Codecommissie komt tot een positief advies.
2. De beoordeling
De advertentie die thans aan de orde is, bevat twee bladzijden. Op de eerste bladzijde
staat een paal met vier borden die allemaal naar rechts wijzen. Op het bovenste bord staat
de naam van het recept, op het bord daaronder staat “geen [antistoffen B] aangetoond”, het
bord daaronder vermeldt “Voorspelbare kosten van [geneesmiddel Z] bij [ziekte C]” terwijl
het laatste en onderste bord het volgende vermeldt “effectief in [D-combinatietherapie]”. De
paal staat tegen een effen blauwe ondergrond. Op de eerste bladzijde is voorts nog
vermeld “3,1 miljoen patiëntjaren klinische ervaring”. De tweede bladzijde behelst verkorte
productinformatie over [geneesmiddel Z].
In de advertentie die in de al genoemde klacht aan de orde was, is verzoekster onder meer
bevolen om het gebruik van de in de klacht in strijd met de Gedragscode geoordeelde
uitingen te staken en om zich voorts te onthouden van het gebruik van uitingen waarin wordt
gesteld dan wel gesuggereerd dat [geneesmiddel Z] superieur is aan een ander met name
genoemd geneesmiddel, zonder dat dit op deugdelijke wijze is onderbouwd. Het eerste bevel
zag in het bijzonder op de afbeelding van een wegbewijzering met daarop aangegeven twee
routes, waarbij de route van [geneesmiddel Z] richting de zon ging en de route van de
[antistoffen B] naar het donker en naar achteren. Voorts was de Codecommissie van oordeel
dat sprake was van vergelijkende reclame tussen [geneesmiddel Z] en andere [medicijnen
E].
De thans aan de orde zijnde folder is anders opgezet. In het bijzonder is er geen
bewegwijzering die naar meerdere kanten wijst en evenmin is sprake van een lichtere en een
donkere kant. In zoverre bestaat geen bezwaar tegen de folder. Nu in de tekst op de borden
evenmin naar andere [medicijnen E] wordt verwezen kan thans niet meer gezegd worden dat
van vergelijkende reclame gesproken moet worden.
De Codecommissie komt op grond van het bovenstaande tot een positief advies.
Moties over (de schijn van) invloed op geneesmiddelenbeleid
%20wikimedia.png) Zes moties: De Kamer, gehoord de beraadslaging,
Zes moties: De Kamer, gehoord de beraadslaging,
29 477, 272
van mening dat iedere schijn van belangenverstrengeling in de zorgsector voorkomen moet worden;
verzoekt de regering, deelname van ambtenaren, toezichthouders en leden van adviesorganen aan farmaceutische lobbyclubs te verbieden,
29 477, 273
constaterende dat binnen het Apollo Netwerk sinds 2007 gesproken wordt over geneesmiddelenbeleid en toetsing van huidig beleid;
constaterende dat de Kamer niet kan controleren in hoeverre het geneesmiddelenbeleid is beïnvloed door dit Apollo Netwerk;
verzoekt de regering, alles wat er binnen het Apollo Netwerk besproken is naar de Tweede Kamer te sturen,
29 477, 274
van mening dat farmalobbyclubs zichzelf kunnen bedruipen;
verzoekt de regering, per direct te stoppen met het sponsoren van farmanetwerken,
29 477, 275
overwegende dat alle (schijn van) beïnvloeding van leden van het College ter Beoordeling van Geneesmiddelen, leden van het College voor zorgverzekeringen, vertegenwoordigers van de Nederlandse Zorgautoriteit en ambtenaren van het ministerie van VWS door farmaceutische bedrijven voorkomen moet worden;
overwegende dat binnen het Apollo Netwerk deze beïnvloeding mogelijk wel plaatsvindt;
verzoekt de regering, er zorg voor te dragen dat leden van het CBG, leden van het CVZ, vertegenwoordigers van de NZa en ambtenaren van het ministerie van VWS in de toekomst niet meer deelnemen aan bijeenkomsten van het Apollo Netwerk,
29 477, 276
overwegende dat ambtenaren van het ministerie van VWS sinds 2007 informele gesprekken voeren met onder anderen vertegenwoordigers van farmaceutische bedrijven in het Apollo Netwerk;
overwegende dat is gebleken dat deze gesprekken van invloed zijn geweest op het door het ministerie van VWS gevoerde beleid;
constaterende dat door de beslotenheid van dit netwerk voor de volksvertegenwoordiging niet te achterhalen is welke invloed hier wordt uitgeoefend door de farmaceutische industrie;
constaterende dat dit netwerk grotendeels gefinancierd wordt door farmaceuten GlaxoSmithKline en Janssen-Cilag;
van mening dat de volksvertegenwoordiging zich op de hoogte moet kunnen stellen van de mate waarin het regeringsbeleid wordt beïnvloed door de farmaceutische industrie;
verzoekt de regering, met de Kamer te delen wat binnen het Apollo Netwerk sinds zijn oprichting in 2007 is besproken en de Kamer onverwijld te informeren over de inhoud van besprekingen binnen dit netwerk in de toekomst,
29 477, 277
overwegende dat transparantie over het Apollo Netwerk bijdraagt aan het voorkomen van de schijn van belangenverstrengeling,
verzoekt de regering, de Tweede Kamer te informeren over de financiële bijdrage die de overige deelnemers vanaf 2007 voor het Apollo Netwerk hebben betaald om zo inzicht te krijgen in de jaarlijkse kosten van dit netwerk,
Antwoord kamervragen over aanbieden geneesmiddelen in onderzoeksstadium
Antwoord kamervragen over het bericht dat de website My Tomorrows geneesmiddelen aanbiedt die zich nog in het onderzoeksstadium bevinden, Aanhangsel Handelingen II, 2013-2014, nr. 1400.%20wikimedia.png) 1. Hoe reageert u op het bericht dat het bedrijf My Tomorrows (MT) geneesmiddelen aanbiedt die zich nog in een onderzoeksstadium bevinden? 1) 2)
1. Hoe reageert u op het bericht dat het bedrijf My Tomorrows (MT) geneesmiddelen aanbiedt die zich nog in een onderzoeksstadium bevinden? 1) 2)
1 My Tomorrows biedt niet zelf geneesmiddelen aan. Daartoe is My Tomorrows ook niet bevoegd. Het initiatief maakt bestaande wettelijke uitzonderingsbepalingen aan een breder publiek bekend en dat kan voor patiënten met een ongeneeslijke ziekte en voor hun behandelaren van belang zijn. Mits My Tomorrows zich houdt aan de wet- en regelgeving, kan dit dus een sympathiek initiatief zijn.
2 Is de wijze waarop MT geneesmiddelen aanbiedt toegestaan? Zo ja, van welke wettelijke mogelijkheden maakt MT gebruik? Zo nee, waarom niet?
Ja. My Tomorrows biedt, zoals gezegd, geneesmiddelen niet zelf aan, maar maakt gebruik van twee uitzonderingen die de wet kent en bemiddelt bij de daarbij behorende procedures. Als hoofdregel is het verboden geneesmiddelen in de handel te brengen zonder vergunning van het College ter beoordeling van geneesmiddelen (CBG). Hierop kent de wet echter enkele uitzonderingen. In de eerste plaats is geen handelsvergunning nodig voor een geneesmiddel dat op uitdrukkelijk schriftelijk initiatief van een arts wordt besteld en dat bestemd is voor individuele patiënten (de zogenaamde ‘named patient’ regeling). Voorafgaand aan de aflevering van dergelijke geneesmiddelen is toestemming van de Inspectie voor de gezondheidszorg (IGZ) vereist.
In de tweede plaats bestaat de mogelijkheid van een zogeheten ‘compassionate use’ programma voor een patiëntengroep, waarvoor het CBG toestemming moet geven. Deze route kan alleen bewandeld worden indien er al een vergunningaanvraag voor het betreffende geneesmiddel in behandeling is genomen. My Tomorrows moet zich ook houden aan de regels voor geneesmiddelenreclame. Reclame voor geneesmiddelen zonder handelsvergunning is verboden, of het nu richting publiek is of richting beroepsbeoefenaren. Op de website van My Tomorrows worden geneesmiddelen niet met name genoemd, dit om de regels inzake geneesmiddelenreclame niet te overtreden. In de uitingen van My Tomorrows is de bewegingsruimte erg beperkt. De IGZ houdt hier toezicht op.
Lees meer hier
Compensatie vertraging KLM staat los van 50%-regeling gastvrijheid
CGR 6 februari 2014, AA14.003 50%-regeling gastvrijheid niet van toepassing. Op de heenvlucht vanuit USA is vertraging ontstaan, waarvoor KLM compensatie heeft aangeboden. Verzoekster verneemt graag of op deze financiële compensatie door KLM de 50 %-regeling voor gastvrijheid van toepassing is en of bij een bevestigende beantwoording van deze vraag verzoekster deze compensatie mag verrekenen in de individuele afrekening voor de kosten van deelneming aan de congresreis danwel de deelnemers moet vragen de compensatie aan verzoekster over te maken.
50%-regeling gastvrijheid niet van toepassing. Op de heenvlucht vanuit USA is vertraging ontstaan, waarvoor KLM compensatie heeft aangeboden. Verzoekster verneemt graag of op deze financiële compensatie door KLM de 50 %-regeling voor gastvrijheid van toepassing is en of bij een bevestigende beantwoording van deze vraag verzoekster deze compensatie mag verrekenen in de individuele afrekening voor de kosten van deelneming aan de congresreis danwel de deelnemers moet vragen de compensatie aan verzoekster over te maken.
Deze vraag beantwoordt de Codecommissie in ontkennende zin. Daarbij is van belang dat de compensatie niet als een vergoeding van reiskosten kan worden aangemerkt. De reis is door de vertraging immers niet duurder geworden voor de deelnemers. Zij zijn vervoerd voor het bedrag dat daarvoor betaald was. Voorts moet worden aangetekend dat de compensatie niet ten laste van verzoekster is gekomen. Zij wordt immers niet door verzoekster maar door KLM betaald. Hoogstens zou kunnen worden gezegd dat de deelnemers door de bedoelde compensatie meer vergoed hebben gekregen voor de deelname aan het congres dan de toegestane 50 % van de kosten van gastvrijheid. Dat moge zo zijn, het gaat de Codecommissie te ver daar het gevolg aan te verbinden dat de deelnemers de compensatie niet zouden mogen behouden. De compensatie is een vergoeding voor de vertraging en het ongemak dat daar het gevolg van is geweest. Het staat in zoverre los van de kosten wegens gastvrijheid waar de Gedragscode op ziet.
Een en ander leidt tot de conclusie dat de 50 %-regeling in deze niet van toepassing is. De tweede door verzoekster gestelde vraag behoeft daarom niet meer te worden beantwoord.
Derdenverzet beschrijvend beslag inzake escitalopram komt ongegrond voor
Voorz. Rechtbank van Koophandel Brussel 12 juni 2012, AR C/12/00101 (NV Sanico tegen Lundbeck)
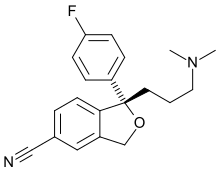 Uitspraak ingezonden door Patricia Cappuyns, Olswang. Derdenverzet. Beslag. Generiek geneesmiddel escitalopram. Derdenverzet door Sanico omdat er prima facie geen geldig recht zou bestaan tot beschrijvende en bewarende maatregelen. Het verweer richt zich hoofdzakelijk tot de inbreuk op de werkwijze conclusie, terwijl de vordering de productconclusie betreft. Het actief bestanddeel van het generieke geneesmiddel is escitalopram dat de productconclusies van het octrooi van deze stof dekt, wat logisch lijkt vermits EUROGENERICS anders zijn generieke marktvergunning zou hebben bekomen. Derdenverzet komt ongegrond voor.
Uitspraak ingezonden door Patricia Cappuyns, Olswang. Derdenverzet. Beslag. Generiek geneesmiddel escitalopram. Derdenverzet door Sanico omdat er prima facie geen geldig recht zou bestaan tot beschrijvende en bewarende maatregelen. Het verweer richt zich hoofdzakelijk tot de inbreuk op de werkwijze conclusie, terwijl de vordering de productconclusie betreft. Het actief bestanddeel van het generieke geneesmiddel is escitalopram dat de productconclusies van het octrooi van deze stof dekt, wat logisch lijkt vermits EUROGENERICS anders zijn generieke marktvergunning zou hebben bekomen. Derdenverzet komt ongegrond voor.
19. (...) Octrooi- en ABC rechten zijn exclusieve rechten die slechts na grondig onderzoek door het EOB worden toegekend. Deze rechten werden door EUROGENERICS noch door SANICO betwist vooraleer met de commercialisatie van het generieke product te beginnen.
Het op de markt brengen van de generieke versie van escitalopram tijdens de beschermingsduur van het ABC'039 wijst op een inbreuk op de exclusieve recht van LUNDBECK.
De voorliggende gegevens lijken er m.a.w. op te wijzen dat de inbreuk op de productconclusie niet redelijkerwijze betwist kan worden en dat er een redelijke kans bestaat dat de producten van EUROGENERICS door de bodemrechter als inbreukmakend zullen worden beschouwd.
Geen vergoeding werkelijke proceskosten
Rechtbank Gelderland 4 december 2013, ECLI:NL:RBGEL:2013:6458 (X tegen Pfizer Manufacturing Belgium NV)
 Schadeposten komen niet onrechtmatig of ongegrond voor en worden toegewezen ad €847.269 (met wettelijke rente vanaf verschillende startdata). Geen vergoeding van de immateriële schade en werkelijke proceskosten. Niet is gesteld of gebleken van misbruik van procesrecht of van anderszins door haar wijze van verweer onrechtmatig handelen jegens eiser.
Schadeposten komen niet onrechtmatig of ongegrond voor en worden toegewezen ad €847.269 (met wettelijke rente vanaf verschillende startdata). Geen vergoeding van de immateriële schade en werkelijke proceskosten. Niet is gesteld of gebleken van misbruik van procesrecht of van anderszins door haar wijze van verweer onrechtmatig handelen jegens eiser.
2.1. Bij op tegenspraak gewezen vonnis van deze rechtbank van 20 januari 2010 is Upjohn veroordeeld aan [eiser] te betalen de als gevolg van het onrechtmatig handelen door hem geleden materiële schade, op te maken bij staat en te vereffenen volgens de wet.
3.2. Het gevorderde komt de rechtbank wat betreft de schadeposten onder B1 t/m B7 en B11 niet onrechtmatig of ongegrond voor en zal daarom worden toegewezen. De over de bedragen sub B1 en B2 gevorderde rente is eveneens toewijsbaar. De over de bedragen sub B3 (€ 44.534,--) en B4 gevorderde rente is toewijsbaar vanaf de datum van betekening van de schadestaat, 6 september 2013, nu [eiser] niet heeft aangegeven tot welke datum de rente in die bedragen is begrepen. De rente over het onder B3 genoemde bedrag van € 3.335,-- is eveneens vanaf laatstbedoelde datum toewijsbaar. Over de bedragen genoemd onder B5, B6, B7 en B11 zal de wettelijke rente eveneens worden toegewezen vanaf 6 september 2013, nu [eiser] niet duidelijk heeft gemaakt wanneer hij de daar genoemde kosten heeft gemaakt/schade heeft geleden.
3.3. De vordering van [eiser] tot vergoeding van immateriële schade (B8) moet worden afgewezen. Op die vordering is al bij vonnis van 20 januari 2010 beslist en thans ligt alleen nog ter beoordeling voor de omvang van de door [eiser] geleden materiële schade, zoals dat ook volgt uit het dictum van laatstbedoeld vonnis.
De rechtbank
4.1. veroordeelt Pfizer om aan [eiser] te betalen een bedrag van € 847.269,-- (zegge: achthonderdzevenenveertigduizend tweehonderd negenenzestig euro), vermeerderd met de wettelijke rente als bedoeld in art. 6:119 BW over:
€ 42.000,-- vanaf 1 januari 2013
€ 101.900,-- vanaf 1 januari 2014
€ 44.534,--, € 3.335,--, € 255.000,--, € 45.000,--, € 250.000,--, € 100.000,-- en € 5.500 vanaf
6 september 2013, telkens tot de dag van volledige betaling,
4.2.
veroordeelt Pfizer in de kosten van de procedure, aan de zijde van [eiser] tot op heden bepaald op € 2.580,-- voor salaris van de advocaat en op € 1.474,-- wegens griffierecht,


















