Geneesmiddelfolders en -brochures zijn verkoopcatalogi die zijn uitgesloten van reclameregelgeving
NL Rechtbank van eerste aanleg Brussel 15 januari 2016, LS&R 1265; eerder als: IEFbe 1693 (verkoopcatalogus Eurogenerics)
 Uitspraak aangebracht door Eric De Gryse, Simont Braun. Het vonnis is in kracht van gewijsde gegaan en dus definitief. Strafrecht. Reclame. Geneesmiddelen. Vrijspraak. Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten stelt in een proces-verbaal dat de door Eurogenerics gehanteerde brochure onder het begrip 'reclame voor geneesmiddelen' valt en niet valt onder de categorie 'verkoopcatalogi en prijslijsten'. Rekeninghoudend met de schikking, vormgeving en inhoud kunnen de folders bestempeld worden als verkoopcatalogi. De in de geviseerde brochures gehanteerde indeling valt niet te beschouwen is als informatie betreffende de geneesmiddelen zodat zij hun status van verkoopcatalogi - die uitgesloten zijn van de reclame-regelgeving - behouden. De rechtbank spreekt de nv Eurogenerics voor de enige tenlastelegging vrij.
Uitspraak aangebracht door Eric De Gryse, Simont Braun. Het vonnis is in kracht van gewijsde gegaan en dus definitief. Strafrecht. Reclame. Geneesmiddelen. Vrijspraak. Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten stelt in een proces-verbaal dat de door Eurogenerics gehanteerde brochure onder het begrip 'reclame voor geneesmiddelen' valt en niet valt onder de categorie 'verkoopcatalogi en prijslijsten'. Rekeninghoudend met de schikking, vormgeving en inhoud kunnen de folders bestempeld worden als verkoopcatalogi. De in de geviseerde brochures gehanteerde indeling valt niet te beschouwen is als informatie betreffende de geneesmiddelen zodat zij hun status van verkoopcatalogi - die uitgesloten zijn van de reclame-regelgeving - behouden. De rechtbank spreekt de nv Eurogenerics voor de enige tenlastelegging vrij.
D.6. Het verbieden van een indeling, zoals door de nv Eurogenerics gehanteerd, zou betekenen dat er geen sprake meer kan zijn van verkoopcatalogi. Er zouden bij wijze van spreken enkel nog alfabetische lijsten mogelijk zijn. Zoals gezegd, is het nochtans inherent aan het begrip verkoopcatalogus dat de koopwaar enigszins wordt 'uitgestald', om de gebruiker een overzicht te bieden van het gamma.
D.7. Er moet besloten worden dat de aan de geviseerde folders geen (gekwalificeerd) verkoopsbevorderend oogmerk ten grondslag ligt, zodat zij het karakter van een verkoopcatalogus behouden.
E. Tweede inbreuk: vermelden van gegevens van de geneesmiddelen
E.1. Zoals uiteengezet, moet het als een inherente eigenschap van een verkoopcatalogus aanvaard worden dat er een indeling wordt gehanteerd om de producten op een efficiënte en praktische wijze voro te stellen.
De indeling in deze zaak heeft een neutrale, objectieve bron en heeft een oriënterend in plaats van een beschrijvend karakter. Indien een dergelijke indeling zou worden beschouwd als het verschaffen van gegevens betreffende de medicamenten, zou de term 'verkoopcatalogus' ieder nuttig effect verliezen.
(...)
E.3. Er moet besloten worden dat de in de geviseerde brochures gehanteerde indeling niet te beschouwen is als informatie betreffende de geneesmiddelen zodat zij hun status van verkoopcatalogi - die uitgesloten zijn van de reclame-regelgeving - behouden.
(...)
Directe octrooiinbreuk door de achter de woorden van de conclusies liggende uitvindingsgedachte
Hof Den Haag 16 februari 2016, LS&R 1265; ECLI:NL:GHDHA:2016:339 (Astrazeneca en Shionogi tegen Resolution)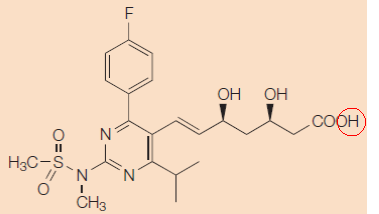
De achter de woorden van de conclusies liggende uitvindingsgedachte
5.3. Bij het achterhalen van de uitvindingsgedachte gaat het om de vaststelling van hetgeen het octrooi toevoegt aan de stand van de techniek en is het perspectief van de gemiddelde vakman en diens kennis van de stand van de techniek op de prioriteitsdatum richtinggevend (vgl. HR in Medinol / Abbott, r.o. 3.5.2). Daarnaast vormen de beschrijving en de tekeningen een belangrijke bron voor het achterhalen van de uitvindingsgedachte (vgl. HR in Medinol / Abbott, r.o. 3.4.2 hiervoor geciteerd). Niet in geschil is dat de gemiddelde vakman in dit geval een organisch chemicus is die zich bezig houdt met de ontwikkeling van nieuwe geneesmiddelen en die in elk geval een basiskennis heeft van de werking van de op de markt zijnde geneesmiddelen zoals rosuvastatine.
5.6. Gelet op de beschrijving in zijn geheel beschouwd, zal de gemiddelde vakman, in aanmerking genomen zijn algemene vakkennis op de prioriteitsdatum, begrijpen dat de uitvinding betrekking heeft op een nieuwe groep van statines – in het bijzonder het specifiek geclaimde rosuvastatine – waarvan de biologische activiteit beter is dan die van een bekende eerste generatie statines. De nieuwheid en inventiviteit van rosuvastatine is niet bestreden. Uitgaand van het perspectief van de gemiddelde vakman op de prioriteitsdatum wordt door het octrooi derhalve een nieuwe groep statines, waaronder meer specifiek rosuvastatine, aan de bekende stand van de techniek toegevoegd. Het vinden daarvan moet worden aangemerkt als de achter de woorden van de conclusie(s) liggende uitvindingsgedachte.
Uitleg van ‘of een niet-toxisch farmaceutisch aanvaardbaar zout daarvan’
5.22. Al het voorgaande leidt tot de conclusie dat de gemiddelde vakman op de prioriteitsdatum geen goede grond had om aan te nemen dat de octrooihouder zijn octrooi wilde beperken tot de in paragraaf 7 genoemde zouten voor gebruik met rosuvastatine en daarmee afstand wilde doen van een deel van de bescherming waarop hij ingevolge de letterlijke bewoordingen van conclusie 1 aanspraak kon maken. Of anders gezegd: de gemiddelde vakman zou niet aannemen dat de octrooihouder er bewust voor heeft gekozen alleen de in paragraaf 7 genoemde zouten van rosuvastatine onder bescherming te stellen. Hij zou de in paragraaf 7 gegeven opsomming daarom niet als limitatief beschouwen. Dat brengt met zich dat conclusie 1 aldus dient te worden uitgelegd dat de beschermingsomvang ervan zich (naast het rosuvastatinezuur) uitstrekt tot alle niet-toxische farmaceutisch aanvaardbare zouten van rosuvastatine, ook die niet zijn genoemd in paragraaf 7 van de beschrijving. Ook onafhankelijk van de ‘goede grond voor afstand-leer’ zou overigens op grond van hetgeen in r.o. 5.14 t/m 5.24 is overwogen tot dezelfde conclusie zijn gekomen.
Toegevoegde materie
5.31. Dat de gemiddelde vakman niet van te voren kon voorspellen of en in welke mate de zuurvorm en zoutvormen van rosuvastatine in de praktijk daadwerkelijk geschikt zouden blijken te zijn voor toepassing in een farmaceutisch preparaat met rosuvastatine, zoals Resolution stelt, staat aan de directe en ondubbelzinnige openbaarmaking in de aanvrage van de in conclusie 1 van EP 471 geclaimde zuurvorm en zoutvormen niet in de weg. Niet-werkende zoutvormen vallen niet onder conclusie 1 omdat daarin alleen farmaceutisch aanvaardbare zouten worden geclaimd. Overigens heeft Resolution, op wie terzake de stelplicht en zo nodig bewijslast rust, onvoldoende onderbouwd aangevoerd op grond waarvan moet worden aangenomen dat de gemiddelde vakman waterstof (waarmee het zuur wordt gevormd), of enig kation waarmee een zout van rosuvastatine gevormd kan worden, ondanks dat deze expliciet in de aanvrage worden genoemd, toch niet als reële mogelijkheid op positie R4 zou meelezen. Ten aanzien van de zuurvorm heeft Resolution gewezen op de publicatie van Berghe uit 1977 ((Pharmaceutical Salts, Journal of Pharmaceutical Sciences, Vol. 66, 1) waarin, niet specifiek ten aanzien van statines, is opgemerkt dat ‘most organic acids and bases are only poorly soluable in H2O’. Dit is evenwel onvoldoende, mede in het licht van de stelling van Astrazeneca, onder verwijzing naar verklaringen van haar partij-deskundigen [S] (3e verklaring par. 3-8 en de daarin genoemde publicatie van T.M. Serajuddin over verschillende statines (Journal of Pharmaceutical Sciences, Vol. 80, 9), waarin is geopenbaard dat polaire statines zoals rosuvastatine als vrij zuur redelijk goed oplosbaar zijn) en [F] (1e verklaring par. 6-11 ), dat de gemiddelde vakman het vrije zuur en een zout als vrijwel gelijk zal beschouwen. Dat conclusie 1 nawerkbaar is heeft Resolution ook niet bestreden.
5.32. Op grond van het voorgaande is het hof van oordeel dat geen sprake is van toegevoegde materie doordat conclusie 1 van EP 471 zich tevens uitstrekt tot rosuvastatinezuur en ook andere niet-toxische farmaceutisch aanvaardbare zouten dan het natrium- en calciumzout.
Gunstbestoon vergunninghouders inzake studiebijeenkomst Davos deels toegestaan
CGR 24 december 2015, LS&R 1263, Advies AA15.109 (Studiebijeenkomst Davos) Verzoekster is voornemens een studiebijeenkomst in Davos te organiseren. Drie vergunninghouders zijn bereidt om hieraan bij te dragen bij wijze van gunstbetoon. Verzoekster vraagt advies over de geoorloofdheid van dit gunstbetoon. De voorgenomen bijdrage door vergunninghouders aan individuele beroepsoefenaren is toelaatbaar. Elke vergunninghouder moet echter, ondanks dit advies, nog wel zelf advies vragen m.b.t. het door haar voorgenomen gunstbetoon. Het advies is negatief voor zover de bijdrage ziet op vergoeding van een deel van de kosten van praktijkondersteuners.
Verzoekster is voornemens een studiebijeenkomst in Davos te organiseren. Drie vergunninghouders zijn bereidt om hieraan bij te dragen bij wijze van gunstbetoon. Verzoekster vraagt advies over de geoorloofdheid van dit gunstbetoon. De voorgenomen bijdrage door vergunninghouders aan individuele beroepsoefenaren is toelaatbaar. Elke vergunninghouder moet echter, ondanks dit advies, nog wel zelf advies vragen m.b.t. het door haar voorgenomen gunstbetoon. Het advies is negatief voor zover de bijdrage ziet op vergoeding van een deel van de kosten van praktijkondersteuners.
Vergelijkende claims AirFluSal in strijd met Gedragscode Geneesmiddelenreclame
CGR Codecommissie 5 februari 2016, LS&R 1262; K15.010 (GlaxoSmithKline tegen Sandoz)
 Uitspraak ingezonden door Machteld Hiemstra, Simmons & Simmons. GSK en Sando zijn ondernemingen die zich bezig houden met de productie, verhandeling en distributie van geneesmiddelen en zijn vergunninghouders zoals in de Gedragscode Geneesmiddelenreclame. Sandoz brengt sinds medio 2015 AirFluSal op de markt, de generieke versie van het merkgeneesmiddel Seretide Diskus van GSK. Deze laatste klaagt over verschillende claims die Sandoz voert ten aanzien van AirFluSal op onder andere een informatiekaartje en in advertenties. De superioriteitsclaims van Sandoz worden volgens GSK door geen enkele vergelijkende klinische studie ondersteund. Zij verzoekt de Codecommissie Sandoz te bevelen het gebruik van de reclamen-uitingen en de claims te staken.
Uitspraak ingezonden door Machteld Hiemstra, Simmons & Simmons. GSK en Sando zijn ondernemingen die zich bezig houden met de productie, verhandeling en distributie van geneesmiddelen en zijn vergunninghouders zoals in de Gedragscode Geneesmiddelenreclame. Sandoz brengt sinds medio 2015 AirFluSal op de markt, de generieke versie van het merkgeneesmiddel Seretide Diskus van GSK. Deze laatste klaagt over verschillende claims die Sandoz voert ten aanzien van AirFluSal op onder andere een informatiekaartje en in advertenties. De superioriteitsclaims van Sandoz worden volgens GSK door geen enkele vergelijkende klinische studie ondersteund. Zij verzoekt de Codecommissie Sandoz te bevelen het gebruik van de reclamen-uitingen en de claims te staken.
De Codecommissie beoordeelt de innovatie claim als vergelijkend en misleidend, nu enig wetenschappelijke onderbouwing daarvan ontbreekt. De geclaimde zichtbare feedback en therapietrouw op zowel de informatiekaart als in de advertentie is eveneens misleidend. De claim is feitelijk onjuist, nu niet duidelijk wordt vermeld dat het noodzakelijk is de strips af te scheuren. De stelling van GSK dat juist het tegenovergestelde van therapietrouw wordt bereikt wordt echter van de hand gewezen, nu dit niet bijdraagt aan het oordeel of de claim juist is. De woorden ‘een nieuwe deur’ zijn niet vergelijkend of misleidend. Sandoz wordt bevolen de met de Gedragscode strijdige uitingen te staken en een rectificatiebrief te verzenden aan haar relaties.
6.8 Met GSK is de Codecommissie eens dat de claim “de bekende combinatie van salmeterol en fluticason, in een nieuwe, innovatieve inhalator: de Forspiro®.” een vergelijking oproept met de Seretide Discus van GSK. Evenzeer moet deze claim als een superioriteitsclaim worden beschouwd. Aan de term “innovatief” moet bij gebruik daarvan in het onderhavige verband niet alleen de betekenis van vernieuwend, maar ook van baanbrekend of grensverleggend worden toegekend, hetgeen impliceert dat de inhalator ten opzichte van andere inhalatoren, zoals de Seretide Discus, een nieuwe therapeutisch relevante functionaliteit bezit, zoals bijvoorbeeld een effectievere werking, een hoger gebruiksgemak of een hogere bijdrage aan therapietrouw. Nu enige wetenschappelijke onderbouwing daarvan ontbreekt, moet de vergelijking reeds om die reden als niet wetenschappelijk aantoonbaar juist worden geacht en moet deze in strijd worden geacht met het bepaalde in artikel 5.2.2.8 van de Gedragscode.
6.11 De Codecommissie stelt vast dat, gegeven de uitleg die Sandoz geeft, voor de geclaimde zichtbare feedback over het aantal per dag gebruikte doses dus kennelijk essentieel is dat per dag de gebruikte strips worden afgescheurd. Nergens in de SmPC of de bijsluiter wordt dit echter vermeld. (…)
6.14 Gezien het hiervoor overwogene is de claim “De Forspiro® laat uw patiënten direct zien of ze vandaag wel of nog niet geïnhaleerd hebben.” feitelijk onjuist, niet in overeenstemming met de SmPC en misleidend en is evenzeer feitelijk onjuist en misleidend de door Sandoz met de uitingen gewekte indruk dat de Forspiro ® innovatief is ten aanzien van gebruiksgemak of therapietrouw. Dit is in strijd met het bepaalde in de artikelen 5.2.2.3 en 5.2.2.8 van de Gedragscode.
6.17 Met betrekking tot de stelling van GSK dat met de AirFluSal Forspiro ® het tegenovergestelde van therapietrouw wordt bereikt, omdat AirFluSal Forspiro alleen beschikbaar is voor de dosering 50/500 µg salmeterol/fluticason en de patiënt zal moeten overschakelen naar een ander middel wanneer de dosering moet worden getitreerd naar de laagste mogelijke dosis (wat ook bij gebruik van AirFluSal Forspiro dient plaats te vinden), hetgeen de therapietrouw niet ten goede komt overweegt de Codecommissie het volgende. Niet ter discussie staat dat AirFluSal Forspiro uitsluitend beschikbaar is in de dosis 50/500 µg salmeterol/fluticason. Die dosering is op zichzelf duidelijk vermeld in de advertentie en ook in de overige promotiematerialen. Ook staat niet ter discussie dat bij de behandeling van patiënten met astma of COPD steeds getitreerd moet worden naar de laagst mogelijke dosering waarbij de symptomen effectief onder controle blijven. Dit staat ook met zoveel woorden in de SmPC en de K15.010 GSK/Sandoz 14 verkorte productinformatie van AirFluSal Forspiro. Als titratie naar een lagere dosering gewenst is, zal een patiënt die AirFluSal Forspiro gebruikt daarom moeten overschakelen naar een ander middel, met een andere inhalator. De Codecommissie is echter van oordeel dat dit aspect niet bijdraagt aan het oordeel dat de onderhavige claim in strijd met de Gedragscode moet worden geacht. Therapietrouw ziet in het algemeen (primair) op het gebruik van het middel volgens voorschrift bij de in de SmPC vermelde indicatie. In zoverre hoeft overschakeling naar een ander product niet af te doen aan therapietrouw.
Bemiddelaar houdt aanspraak op provisie gedurende looptijd mantelcontract, ook na voortijdige opzegging
Hof Arnhem-Leeuwarden 2 februari 2016, LS&R 1261; ECLI:NL:GHARL:2016:621 (appellante tegen VGZ) Centrale vraag is of appellante, ook nadat zij geen werkzaamheden meer uitvoerde voor het mantelcontract t.b.v. Oracle, nog aanspraak kon maken jegens VGZ op provisie op grond van de samenwerkingsovereenkomst. De rechtbank beantwoordde deze vraag eerder ontkennend. Voor beantwoording is uitleg van de samenwerkingsovereenkomst tussen zorgverzekeraar en bemiddelaar noodzakelijk, met name uitleg van het begrip “bemiddeling”. Partijen hebben onvoldoende gesteld dat er sprake is van een éénduidig gebruik van het begrip “bemiddeling” in de branche. Het hof komt tot het oordeel dat artikel 7 van de samenwerkingsovereenkomst zo moet worden uitgelegd dat voor [appellante] aanspraak op provisie bestaat voor de door haar verrichte bemiddeling ter zake het mantelcontract gedurende de looptijd van dat mantelcontract. Het bestreden arrest wordt vernietigd en de vordering toegewezen.
Centrale vraag is of appellante, ook nadat zij geen werkzaamheden meer uitvoerde voor het mantelcontract t.b.v. Oracle, nog aanspraak kon maken jegens VGZ op provisie op grond van de samenwerkingsovereenkomst. De rechtbank beantwoordde deze vraag eerder ontkennend. Voor beantwoording is uitleg van de samenwerkingsovereenkomst tussen zorgverzekeraar en bemiddelaar noodzakelijk, met name uitleg van het begrip “bemiddeling”. Partijen hebben onvoldoende gesteld dat er sprake is van een éénduidig gebruik van het begrip “bemiddeling” in de branche. Het hof komt tot het oordeel dat artikel 7 van de samenwerkingsovereenkomst zo moet worden uitgelegd dat voor [appellante] aanspraak op provisie bestaat voor de door haar verrichte bemiddeling ter zake het mantelcontract gedurende de looptijd van dat mantelcontract. Het bestreden arrest wordt vernietigd en de vordering toegewezen.
4.5 Gelet op de hiervoor geschetste wijze van totstandkoming van de samenwerkingsovereenkomst, waarvan vast staat dat die éénzijdig door VGZ is opgesteld zonder dat [appellante] daarop invloed heeft uitgeoefend, komt naast de tekst van de overeenkomst gewicht toe aan de specifieke achtergrond van de overeenkomst, de wijze van totstandkoming daarvan en de verhouding tussen partijen. Dit geldt te meer nu onvoldoende is gesteld en onderbouwd om aan te nemen dat sprake is van een éénduidig gebruik van het begrip “bemiddeling” in de branche. Beide partijenstellen weliswaar dat de eigen uitleg van de overeenkomst gebruikelijk is in de branche, maar zij onderbouwen dit geen van beiden in voldoende mate. Uit de overgelegde (delen van) contracten met andere verzekeraars dan VGZ blijkt weliswaar dat een aantal verzekeraars in hun afspraken met bemiddelaars als regel hanteert dat bij overgang van een verzekering op verzoek van de klant de oude bemiddelaar aanspraak blijft houden op provisie tot de eerstvolgende vervaldatum van het verzekeringscontract van die klant. Onduidelijk is echter of dit alle zorgverzekeraars betreft. Uit die stukken blijkt ook dat ONVZ en Achmea in hun contracten met bemiddelaars uitdrukkelijk bepalen dat deze regel ook geldt voor collectieve ziektekostenverzekeringen, met dien verstande dat dan de vervaldatum van het collectieve contract wordt gehanteerd als einddatum voor de aanspraak op provisie. In de overgelegde stukken afkomstig uit contracten met andere verzekeraars valt niet te lezen dat deze regel daar ook wordt toegepast op mantelcontracten.
4.6 Op grond van nadere beschouwing van de hiervoor onder 4.3 geschetste achtergronden van de samenwerkingsovereenkomst, de wijze van totstandkoming van die overeenkomst en de verhouding tussen partijen komt het hof tot het oordeel dat artikel 7 van de samenwerkingsovereenkomst zo moet worden uitgelegd dat voor [appellante] aanspraak op provisie bestaat voor de door haar verrichte bemiddeling ter zake het mantelcontract gedurende de looptijd van dat mantelcontract. Daarvoor is het volgende van belang.
In de memorie van grieven en tijdens het pleidooi in hoger beroep is door [appellante] betoogd dat provisie (in het algemeen en in dit geval) niet gelijk te stellen valt met rechtstreekse beloning, in die zin dat er niet noodzakelijkerwijze een rechtstreeks verband bestaat tussen de aanspraak op provisie (die vaak gebaseerd is op de hoogte van de verzekeringspremie) en de door de bemiddelaar voor de individuele klant te verrichten werkzaamheden. Dit vanwege het feit dat minder bewerkelijke klanten de werkzaamheden voor bewerkelijke klanten als het ware subsidiëren en de bemiddelaar met de totale jaarlijkse provisie die binnenkomt ook alle advieswerkzaamheden moet bekostigen voor (potentiële) klanten die uiteindelijk geen verzekering afsluiten via de bemiddelaar. VGZ heeft de strekking van dit betoog niet betwist en daarmee gaan haar argumenten niet op, voor zover die zijn gebaseerd op de stelling dat [appellante] geen aanspraak meer heeft op provisie omdat zij na 1 januari 2014 (noodgedwongen) geen werkzaamheden meer ter zake het mantelcontract heeft uitgevoerd.
Afgezien daarvan heeft [appellante] voldoende aannemelijk gemaakt, zoals blijkt uit het hiervoor onder 4.3 weergegevene, dat het zwaartepunt van haar werkzaamheden lag in het totstandbrengen van het mantelcontract, hetgeen rijmt met haar uitleg dat de looptijd van de provisieregeling gekoppeld is aan de looptijd van dat mantelcontract. Vast staat dat die looptijd 3 jaar bedraagt en dat door VGZ en Oracle, na bemiddeling door [appellante], bewust is gekozen voor die langere looptijd, omdat die zowel gunstig was voor VGZ als voor Oracle. In het mantelcontract is voorts niet voorzien in een tussentijdse opzegging door Oracle, terwijl noch in de samenwerkingsovereenkomst, noch in de bijlage is geregeld dat de provisie voor [appellante] stopt bij tussentijdse opzegging door de klant (in dit geval Oracle).
Vordering tot betaling achterstallig honorarium volledig toegewezen, ondanks onenigheid opzegtermijn
Vzr. Rechtbank Gelderland 18 januari 2016, LS&R 1260; ECLI:NL:RBGEL:2016:596 (eiser tegen A-Klinieken) Eiser, medisch specialist plastische chirurgie, heeft toelatingsovereenkomsten gesloten met Semper Fidelis en Stichting A-Klinieken. Na de beëindiging vordert eiser betaling van achterstallig honorarium. A-Klinieken is het eens met de vordering, maar stelt enkele tegenvorderingen te hebben. Onder meer vanwege het niet in acht nemen van de opzegtermijn door eiser. Zij vordert in reconventie wordt voorschot op schadevergoeding op grond van onregelmatige opzegging en wanprestatie. De rechter wijst honorarium vanwege bereikte overeenstemming over verschuldigde bedrag toe. Er zijn voldoende aanwijzingen dat A-Klinieken heeft geaccepteerd dat eiser zonder inachtneming van de opzegtermijn zou vertrekken. Voor beoordeling schadevergoedingsvordering op grond van wanprestatie leent het kort geding zich niet. Afwijzing beroep op verrekening en reconventie.
Eiser, medisch specialist plastische chirurgie, heeft toelatingsovereenkomsten gesloten met Semper Fidelis en Stichting A-Klinieken. Na de beëindiging vordert eiser betaling van achterstallig honorarium. A-Klinieken is het eens met de vordering, maar stelt enkele tegenvorderingen te hebben. Onder meer vanwege het niet in acht nemen van de opzegtermijn door eiser. Zij vordert in reconventie wordt voorschot op schadevergoeding op grond van onregelmatige opzegging en wanprestatie. De rechter wijst honorarium vanwege bereikte overeenstemming over verschuldigde bedrag toe. Er zijn voldoende aanwijzingen dat A-Klinieken heeft geaccepteerd dat eiser zonder inachtneming van de opzegtermijn zou vertrekken. Voor beoordeling schadevergoedingsvordering op grond van wanprestatie leent het kort geding zich niet. Afwijzing beroep op verrekening en reconventie.
Vorderingen op grond van goodwill bepalingen koopovereenkomst apotheek afgewezen
Rechtbank Midden-Nederland 27 januari 2016, LS&R 1259; ECLI:NL:RBMNE:2016:343 (eiseres tegen Dorestede de Horden) Overdracht goodwill apotheek. Uitleg contractuele bepalingen. Eiseres en Dorestede zijn de overdracht van de apotheek van eiseres overeengekomen. In de overeenkomst wordt een voorwaardelijke geldbetaling opgenomen. Indien 70% van de recepten voortkomt uit Proactief en/of Reactief en wanneer van het klantenbestand 70% van de mobiele nummers beschikbaar zijn en ingevoerd in de kluisjesmodule, is Koper voor beide gevallen 40.000 euro verschuldigd aan Verkoper. Eiseres vordert betaling van de 80.000 euro, maar Dorestede stelt dat niet aan de eisen van deze resultaatverbintenissen is voldaan. De rechter gaat hierin mee. Aan de eerste eis is niet voldaan, nu 70% van het Proactief/Reactief herhalen via de website moest gebeuren. Dit was uit oogpunt van efficiëntie een belangrijke eis waaraan niet is voldaan. Wat betreft de eis van 70% stelt eiseres dat deze is behaald nu het alleen zou gaan om patiënten uit de vestigingsplaats. Dit standpunt heeft zij eveneens onvoldoende onderbouwd, nu de bepaling de strekking had om zoveel mogelijk patiënten een sms te kunnen sturen. De vorderingen worden afgewezen.
Overdracht goodwill apotheek. Uitleg contractuele bepalingen. Eiseres en Dorestede zijn de overdracht van de apotheek van eiseres overeengekomen. In de overeenkomst wordt een voorwaardelijke geldbetaling opgenomen. Indien 70% van de recepten voortkomt uit Proactief en/of Reactief en wanneer van het klantenbestand 70% van de mobiele nummers beschikbaar zijn en ingevoerd in de kluisjesmodule, is Koper voor beide gevallen 40.000 euro verschuldigd aan Verkoper. Eiseres vordert betaling van de 80.000 euro, maar Dorestede stelt dat niet aan de eisen van deze resultaatverbintenissen is voldaan. De rechter gaat hierin mee. Aan de eerste eis is niet voldaan, nu 70% van het Proactief/Reactief herhalen via de website moest gebeuren. Dit was uit oogpunt van efficiëntie een belangrijke eis waaraan niet is voldaan. Wat betreft de eis van 70% stelt eiseres dat deze is behaald nu het alleen zou gaan om patiënten uit de vestigingsplaats. Dit standpunt heeft zij eveneens onvoldoende onderbouwd, nu de bepaling de strekking had om zoveel mogelijk patiënten een sms te kunnen sturen. De vorderingen worden afgewezen.
4.1. Artikel 7.4 onder a van de koopovereenkomst, bezien in combinatie met artikel 7.5, stelt als voorwaarde voor een aanvullende betaling van € 40.000 aan [eiseres] dat op 31 juli 2014 70% van de recepten voort moest komen uit proactief en/of reactief herhalen via de website (zie 2.5). [eiseres] heeft gedeeltelijk niet voldaan aan deze voorwaarde, namelijk wat betreft de eis ‘via de website’. Volgens [eiseres] heeft zij toch voldaan aan de in artikel 7.4 onder a gestelde voorwaarde omdat a) minstens 70% van de recepten voortkwam uit proactief en/or reactief en b) partijen met artikel 7.4 de bedoeling hebben gehad te bewerkstelligen dat na de overname van de apotheek door Dorestede zoveel mogelijk patiënten, en daarmee omzet, voor Dorestede behouden zouden blijven. [eiseres] stelt dat Dorestede (nagenoeg) alle patiënten heeft behouden en dat de omzet minstens gelijk is gebleven. Daarmee heeft zij volgens haar voldaan aan de bedoeling van partijen.
4.4. Als partijen uitsluitend behoud van patiënten en omzet hadden beoogd, had kunnen worden volstaan met de formulering ‘zodra voor koper aantoonbaar is gebleken dat 70% van de recepten voortkomt uit proactief en/of reactief herhalen’ en had de aanvullende voorwaarde, dat dit ‘via de website’ moest gaan, weggelaten kunnen worden. Het is aannemelijk dat, zoals Dorestede aanvoert, deze aanvullende voorwaarde door Dorestede is gesteld uit oogpunt van efficiëntie, en [eiseres] ( [A] ) heeft dat kunnen en moeten begrijpen.
4.5. Daarnaast bestond de werkwijze van de door [eiseres] aan patiënten verstrekte service van herhaalrecepten, met welke werkwijze [A] als beherend apotheker van Dorestede is doorgegaan tot en met 31 juli 2014, er deels uit dat patiënten lege doosjes, waarin door hen gebruikte geneesmiddelen hadden gezeten, bij [A] inleverden, waarna hij zonder recept die geneesmiddelen verstrekte aan die patiënten. [A] deed dit op grond van een afspraak met de huisartsen en die verstrekkingen werden dan achteraf door de huisartsen geparafeerd. Dorestede stelt dat deze werkwijze voor uitdeelposten wettelijk is verboden en dat de apotheek, die via een uitdeelpost geneesmiddelen verstrekt, eerst een recept moet hebben. [eiseres] heeft deze stelling niet weersproken, zodat zij vast staat. Door via de website te werken zou zich dit probleem niet voordoen bij Dorestede en aangenomen moet worden dat dit [eiseres] bij het sluiten van de koopovereenkomst duidelijk was.
4.9 Volgens [eiseres] had zij op 31 juli 2014 van 1373 patiënten de mobiele telefoonnummers ingevoerd in de kluisjesmodule. Bij een klantenbestand van 2367 patiënten komt dit neer op 58% van het totaal. Toch stelt [eiseres] dat zij wel aan artikel 7.4 onder b van de koopovereenkomst heeft voldaan. In verband hiermee betoogt zij dat het de bedoeling van partijen was dat 70% van de mobiele telefoonnummers van de in [vestigingsplaats] woonachtige patiënten van haar apotheek op 31 juli 2014 voor Dorestede beschikbaar moest zijn en ingevoerd in de kluisjesmodule. Volgens [eiseres] heeft zij aan deze voorwaarde voldaan omdat 1373 patiënten van haar apotheek op 31 juli 2014 de code PC (Pharmaself [vestigingsplaats] ) hadden en van al haar patiënten er 1905 in [vestigingsplaats] woonachtig waren. Dit brengt volgens [eiseres] mee dat voor 72% van het beoogde totale aantal patiënten de mobiele telefoonnummers waren ingevoerd in de kluisjesmodule van Pharmacom. Ter onderbouwing hiervan voert [eiseres] aan dat zij, kennelijk voor 30 juli 2014, mondeling van Dorestede de instructie heeft gekregen dat alleen inwoners van [vestigingsplaats] en niet van omringende plaatsen mochten worden overgezet naar PC. Die instructie impliceerde dat een patiënt uit Langbroek geneesmiddelen ook in Langbroek kon afhalen en een patiënt uit Wijk bij Duurstede zijn geneesmiddelen in die plaats kon afhalen. Volgens [eiseres] blijkt deze instructie ook uit de e-mail van [D] van 30 juli 2014 (zie 2.13). Verzocht een patiënt uit Langbroek eenmalig dat hij zijn geneesmiddelen in [vestigingsplaats] kon ophalen, bijvoorbeeld omdat hij toch in [vestigingsplaats] moest zijn, dan werd zijn code in het automatiseringssysteem van Dorestede tijdelijk door [A] omgezet naar PC.4.17 Daarnaast is de rechtbank ook met betrekking tot de in artikel 7.4 onder b genoemde voorwaarde van oordeel dat [eiseres] , anders dan [eiseres] betoogt, niet heeft voldaan aan deze voorwaarde omdat, zoals zij stelt, de onderliggende bedoeling van partijen uitsluitend te bewerkstelligen dat de patiënten en omzet voor Dorestede zouden blijven. Ook in dit verband geldt dat, als dit uitsluitend de bedoeling was, het in dat geval overbodig zou zijn geweest om artikel 7.4 onder b in de overeenkomst op te nemen. Deze bepaling had (mede) de strekking te bewerkstelligen dat zoveel mogelijk patiënten een sms konden ontvangen met de mededeling dat zij hun geneesmiddel bij de afhaalmachine kunnen ophalen (zie 2.12). Ook hier ligt voor de hand dat, zoals Dorestede aanvoert, deze voorwaarde door Dorestede is gesteld uit oogpunt van efficiëntie. Zonder deze mogelijkheid zou Dorestede de patiënten immers zelf moeten bellen of e-mailen om hen erop te wijzen dat zij hun geneesmiddel bij de afhaalmachine kunnen ophalen, of zou Dorestede zelf alle mobiele telefoonnummers in de kluisjesmodule hebben moeten invoeren. [eiseres] ( [A] ) heeft dat kunnen en moeten begrijpen.
HR over uitleg regel ‘disclosed but not claimed is disclaimed'
HR 5 februari 2016, LS&R 1258; ECLI:NL:HR:2016:196 (Bayer Pharma tegen Sandoz) Octrooirecht. Farmaceutisch octrooi; Bereidingswijze van drospirenon (werkzame stof in een anticonceptiepil). Zie eerder IEF 15380 (concl. AG) IEF 13391 (Hof) en IEF 12275 (Rb). Art. 69 EOV en Uitlegprotocol. Equivalente maatregelen. Maatstaf. Reikwijdte van de regel ‘Disclosed but not claimed is disclaimed’. De Hoge Raad verwerpt het beroep en veroordeelt Bayer in de kosten van Sandoz in cassatie (ad €130.000).
Octrooirecht. Farmaceutisch octrooi; Bereidingswijze van drospirenon (werkzame stof in een anticonceptiepil). Zie eerder IEF 15380 (concl. AG) IEF 13391 (Hof) en IEF 12275 (Rb). Art. 69 EOV en Uitlegprotocol. Equivalente maatregelen. Maatstaf. Reikwijdte van de regel ‘Disclosed but not claimed is disclaimed’. De Hoge Raad verwerpt het beroep en veroordeelt Bayer in de kosten van Sandoz in cassatie (ad €130.000).
(HOF) 4.20 Het voorgaande samengevat: de gemiddelde vakman wist dat er vele methoden waren om oxidatie van alcoholgroepen in ZK92836 te bewerkstelligen, waaronder het gebruik van TEMPO. De gemiddelde vakman ging er echter niet van uit dat de met een rutheniumzout bereikte selectiviteit van 5ß-OH-DRSP en mate van terugdringing van bepaalde bijproducten ook zou kunnen worden verkregen met behulp van TEMPO. Voorshands moet daarom - ook onder het uitgangspunt dat rutheniumzout-gekatalyseerde oxidatie geen essentieel kenmerk is van de in WO 738/EP 791 geopenbaarde uitvinding - worden geoordeeld dat in de ogen van de gemiddelde vakman de aanvrager van EP 791 omwille van deze aan rutheniumzout verbonden voordelen bewust voor die stof heeft gekozen uit de vele hem ten dienste staande mogelijkheden, althans dat hij omwille van die voordelen bewust voor rutheniumzout heeft gekozen boven TEMPO.
(HR)
3.3.6
Voor zover onderdeel 1.1.1 het hof verwijt de regel te hebben miskend dat de maatstaf voor het niet beschermen van equivalente maatregelen daarin gezocht moet worden dat een goede grond ervoor moet bestaan dat de octrooihouder afstand heeft gedaan van die bescherming, hoewel hij die had kunnen verkrijgen, gaat het uit van een opvatting die geen steun vindt in het recht. Het hof heeft terecht onderzocht of de gemiddelde vakman uit conclusie 1 van EP 791 zou begrijpen dat de octrooihouder in de oxidatiestap een bewuste keuze heeft gemaakt voor het gebruik van rutheniumzout als katalysator. Daartoe heeft het hof in aanmerking genomen: de inhoud van het octrooi, de stand van de techniek, het met de geoctrooieerde werkwijze beoogde doel, de bijkomende voordelen van die werkwijze, de kennis van het bestaan van de betrokken stoffen, de aard van en de verhouding tussen die stoffen, alsmede de mate en wijze waarin zij tot het beoogde resultaat leiden, dit alles vanuit het perspectief van de gemiddelde vakman. Het wegen van al deze omstandigheden heeft het hof tot het oordeel gebracht (samengevat in rov. 4.20) dat Bayer bewust voor rutheniumzout heeft gekozen, zodat het gebruik van tempo als katalysator geen inbreuk maakt op EP 791. Dit oordeel berust op een aan het hof voorbehouden weging van relevante factoren en is niet onbegrijpelijk of ontoereikend gemotiveerd.
3.3.7
Onderdeel 1.1.2 ziet om te beginnen eraan voorbij dat uit rov. 4.19 volgt dat naar het oordeel van het hof voor de gemiddelde vakman tempo niet een stof was waarmee hetzelfde resultaat bereikt kon worden als met rutheniumzout, zodat reeds daarom niet van equivalentie sprake kan zijn. Voorts miskent het dat het bij de hier aan de orde zijnde vraag erom gaat of in de perceptie van de gemiddelde vakman de conclusies, gelezen in het licht van de beschrijving en de tekeningen, ruimte laten voor equivalenten, gelet op enerzijds een adequate bescherming van de octrooihouder en anderzijds de rechtszekerheid voor derden. Daarbij speelt de wil of de bedoeling van de aanvrager om van die bescherming afstand te doen, geen beslissende rol. Voor het overige bouwen de klachten van onderdeel 1.1.2, evenals die van onderdeel 1.1.3, voort op die van onderdeel 1.1.1, zodat die het lot daarvan moeten delen.
3.3.8
Onderdeel 1.2 klaagt over de door het hof gehanteerde peildatum voor de beschermingsomvang. Volgens het onderdeel heeft het hof bij de beantwoording van de vraag hoe de gemiddelde vakman het octrooi zal begrijpen, ten onrechte (uitsluitend) de prioriteits- of verleningsdatum als peildatum voor de kennis van de gemiddelde vakman gehanteerd. Volgens het onderdeel is bij die beoordeling maatgevend, althans mede bepalend, wat de kennis van de gemiddelde vakman is ten tijde van de (voorbereidingen op de) gestelde inbreuk.
Ook dit onderdeel slaagt niet. Voor het bepalen van de beschermingsomvang van een octrooi gaat het om de vaststelling van hetgeen het octrooi toevoegt aan de stand van de techniek. Alleen in het kader van de inbreukvraag kan mede betekenis worden gehecht aan de kennis van de gemiddelde vakman ten tijde van de beweerde inbreuk, in het bijzonder waar het erom gaat of sprake is van equivalente elementen (HR 4 april 2014, ECLI:HR:2014:816, NJ 2015/11 (Medinol/Abbott), rov. 3.5.2).
3.3.9
De overige in onderdeel 1 aangevoerde klachten kunnen evenmin tot cassatie leiden. Dit behoeft, gezien art. 81 lid 1 RO, geen nadere motivering nu de klachten niet nopen tot beantwoording van rechtsvragen in het belang van de rechtseenheid of de rechtsontwikkeling.
Inbreuk op EP 840?
3.4.1
Onderdeel 2 richt zich tegen rov. 5.5-5.10, die betrekking hebben op EP 840, waarin het hof heeft onderzocht of het gebruik van een base voor waterafsplitsing equivalent is aan dat van het geclaimde specifieke zuur pTSA. In rov. 5.5 is overwogen dat in de beschrijving op niet mis te verstane wijze wordt geopenbaard dat 5β-OH-DRSP labiel is onder zure en basische omstandigheden en dat het dus niet alleen onder invloed van het zuur pTSA, maar ook onder invloed van andere (Lewis)zuren en onder invloed van basen uiteenvalt in water en DRSP. De gemiddelde vakman zal dan aannemen dat voor de in de beschrijving wel geopenbaarde, maar niet in de conclusie geclaimde middelen geen bescherming wordt gezocht (‘disclosed but not claimed is disclaimed’). Dan brengt de rechtszekerheid een restrictieve uitleg mee: onder het octrooi valt alleen het gebruik van pTSA en in elk geval niet het gebruik van een base als pyridine (rov. 5.6).
Deze uitleg wordt (volgens rov. 5.7) verder ondersteund door het feit dat de conclusies volgens het verleningsdossier in oppositie zijn teruggebracht tot één overgebleven conclusie met alleen pTSA, waaruit derden konden afleiden dat afstand was gedaan van, althans geen bescherming was verleend voor andere middelen/methoden, alsmede door het gegeven (rov. 5.8) dat Bayer in een afgesplitste aanvrage het gebruik van een base claimt voor waterafsplitsing. In rov. 5.9 overweegt het hof dat het oordeel van de examiner dat EP 840/WO 738 geen basis biedt voor een conclusie met een basische waterafsplitsing in het kader van een art. 123(2) EOV kwestie er niet aan afdoet dat gebruik van basen in het algemeen zodanig duidelijk is geopenbaard in de beschrijving van EP 840, dat de hier in het kader van art. 69 EOV te maken afweging in het nadeel van Bayer uitvalt.
3.4.2 Onderdeel 2.1.1 betoogt dat van toepassing van de in rov. 5.5 vermelde regel ‘disclosed but not claimed is disclaimed’ geen sprake kan zijn als de ‘openbaring’ niet betrekking heeft op een middel dat de basis kan vormen voor een conclusie. Deze klacht berust op een onjuiste rechtsopvatting, zoals reeds valt af te leiden uit HR 25 mei 2012, ECLI:NL:HR:2012:BV3680, NJ 2013/68 (AGA/Occlutech).De door het onderdeel bepleite opvatting komt neer op het weginterpreteren van het slot van de conclusie van EP 840, waarmee deze niet anders zou leren dan dat op enigerlei bekende wijze waterafsplitsing dient plaats te vinden, terwijl de wijze van waterafsplitsing onderdeel van de uitvinding is. Daarom faalt de klacht. De onderdelen 2.1.2 en 2.1.3 bouwen voort op onderdeel 2.1.1 en missen daarom eveneens doel.
3.4.3 Onderdeel 2.1.4 faalt op de gronden, vermeld in de conclusie van de Advocaat-Generaal onder 3.20. Onderdeel 2.1.5 mist zelfstandige betekenis.
3.4.4 Nu het oordeel van het hof reeds steunt op de tevergeefs bestreden rov. 5.5 en 5.6, kunnen de tegen rov. 5.7-5.10 gerichte klachten (onderdelen 2.2 en 2.3) bij gebrek aan belang niet tot cassatie leiden.
Onderdeel 3 bevat geen zelfstandige klacht.
Uitbater café zelf verantwoordelijk voor stroken drank- en horecavergunning met feitelijke situatie
CBb 29 december 2015, LS&R 1257; ECLI:NL:CBB:2015:443 (appellant tegen Minister van VWS) Tabakswet. Bij inspectie heeft een ambtenaar van de NVWA een overtreding van het rookverbod geconstateerd in de horecagelegenheid van appellant. Op grond hiervan legt de minister een bestuurlijk boete op. De rechtbank heeft het beroep ongegrond verklaard en stelt dat de minister terecht is uitgegaan van het in de drank- en horecawetvergunning vermelde vloeroppervlak van 106m2. Appellant maakt hiertegen bezwaar. Tijdens het onderzoek was immers een deel van de horecagelegenheid afgesloten waardoor het oppervlak slechts 70m2 bedroeg. Het College is met de rechtbank van oordeel dat de enkele constatering dat een deel was afgesloten onvoldoende is om te concluderen dat dit deel niet moet worden aangemerkt als onderdeel van de horecalokaliteit. Appellant is zelf verantwoordelijk om ervoor te zorgen dat zijn drank- en horecavergunning is overeenstemming is met de feitelijke situatie.
Tabakswet. Bij inspectie heeft een ambtenaar van de NVWA een overtreding van het rookverbod geconstateerd in de horecagelegenheid van appellant. Op grond hiervan legt de minister een bestuurlijk boete op. De rechtbank heeft het beroep ongegrond verklaard en stelt dat de minister terecht is uitgegaan van het in de drank- en horecawetvergunning vermelde vloeroppervlak van 106m2. Appellant maakt hiertegen bezwaar. Tijdens het onderzoek was immers een deel van de horecagelegenheid afgesloten waardoor het oppervlak slechts 70m2 bedroeg. Het College is met de rechtbank van oordeel dat de enkele constatering dat een deel was afgesloten onvoldoende is om te concluderen dat dit deel niet moet worden aangemerkt als onderdeel van de horecalokaliteit. Appellant is zelf verantwoordelijk om ervoor te zorgen dat zijn drank- en horecavergunning is overeenstemming is met de feitelijke situatie.
3.7 Het College is met de rechtbank van oordeel dat de enkele constatering dat de (voormalige) rookruimte ten tijde van de inspectie niet in gebruik was, onvoldoende is om de conclusie te dragen dat deze ruimte – gelet op de definitie die is gegeven in artikel 1, sub c, van het Besluit – niet moet worden aangemerkt als (onderdeel van de) horecalokaliteit waarin appellant zijn horecabedrijf uitoefende. De minister heeft in dat verband terecht opgemerkt dat appellant bij een ongewijzigde drank- en horecawetvergunning, vrijelijk over genoemde (rook)ruimte kon beschikken en daarin op ieder gewenst moment zijn horecabedrijf kon uitoefenen in die zin dat hij in genoemde ruimte alcoholhoudende drank kon verstrekken voor gebruik ter plaatse. Het College kan dit gebruik van de (voormalige) rookruimte door appellant geenszins uitsluiten, nu gesteld noch gebleken is dat de toegangsdeuren tot genoemde ruimte waren gebarricadeerd dan wel dat appellant die ruimte anderszins permanent ontoegankelijk had gemaakt voor cafébezoekers. Bovendien blijkt uit het proces-verbaal dat genoemde ruimte ten tijde van de inspectie nog altijd met tafels en stoelen was ingericht. Voor zover al ervan moet worden uitgegaan dat de (voormalige) rookruimte en de caféruimte waar de bar zich bevindt samen één enkele horecalokaliteit (als bedoeld in artikel 3, tweede lid, in het Besluit) vormen in plaats van twee afzonderlijke horecalokaliteiten, onderschrijft het College het oordeel van de rechtbank dat ook het vloeroppervlak van de (voormalige) rookruimte moet worden betrokken bij de berekening van de totale oppervlakte van de horecalokaliteit. De conclusie luidt daarom dat de uitzondering op het rookverbod als neergelegd in artikel 3, tweede lid, van het Besluit niet op appellant van toepassing is.
Beweerdelijke schade door publicatie geen reden om bestuursrechtelijke boetes te verlagen
CBb 29 december 2015, LS&R 1256; ECLI:NL:CBB:2015:442 (appellante tegen Minister van VWS) Warenwet. Bij inspectie hebben ambtenaren van de NVWA verschillende overtredingen van de Warenwet geconstateerd bij het strandpaviljoen van appellante. Het strandpaviljoen wordt gesloten en de minister legt twee boetes op. De NVWA publiceert hierover een bericht op haar online media. Appellante maakt bezwaar tegen de boetebesluiten en stelt dat de publicatie onrechtmatig is. De rechtbank verklaard het beroep ongegrond. Het College ziet in hetgeen appellante aanvoert onvoldoende aanleiding om te oordelen dat de minister in redelijkheid niet van die bevoegdheid gebruik heeft kunnen maken, dan wel dat de hoogte van de opgelegde boetes verlaagd dient te worden. Aan de schade die appellante stelt te lijden als gevolg van de publicatie over de sluiting kan hier geen nadere betekenis toekomen. Zij kan haar schade aan de burgerlijke rechter voorleggen. Het hoger beroep wordt ongegrond verklaard.
Warenwet. Bij inspectie hebben ambtenaren van de NVWA verschillende overtredingen van de Warenwet geconstateerd bij het strandpaviljoen van appellante. Het strandpaviljoen wordt gesloten en de minister legt twee boetes op. De NVWA publiceert hierover een bericht op haar online media. Appellante maakt bezwaar tegen de boetebesluiten en stelt dat de publicatie onrechtmatig is. De rechtbank verklaard het beroep ongegrond. Het College ziet in hetgeen appellante aanvoert onvoldoende aanleiding om te oordelen dat de minister in redelijkheid niet van die bevoegdheid gebruik heeft kunnen maken, dan wel dat de hoogte van de opgelegde boetes verlaagd dient te worden. Aan de schade die appellante stelt te lijden als gevolg van de publicatie over de sluiting kan hier geen nadere betekenis toekomen. Zij kan haar schade aan de burgerlijke rechter voorleggen. Het hoger beroep wordt ongegrond verklaard.
5.1 Het College stelt vast dat appellante de overtredingen die aan de boetebesluiten ten grondslag liggen, niet betwist. Evenmin staat ter discussie dat de geconstateerde overtredingen bij wettelijk voorschrift met een gefixeerd boetebedrag zijn gesanctioneerd. In zoverre is dus niet in geschil dat de minister in beginsel over de bevoegdheid beschikt om appellante de boetebesluiten op te leggen. Het College ziet in hetgeen appellante aanvoert onvoldoende aanleiding om te oordelen dat de minister in redelijkheid niet van die bevoegdheid gebruik heeft kunnen maken, dan wel dat de hoogte van de opgelegde boetes ingevolge artikel 5:46, derde lid, van de Algemene wet bestuursrecht verlaagd dient te worden. Daartoe overweegt het College als volgt.
5.2 Anders dan appellante betoogt, is het College van oordeel dat aan de schade die appellante stelt te lijden als gevolg van de publicatie over de sluiting, in het kader van de verdere bestuursrechtelijke besluitvorming van de minister, zoals de oplegging van de boetebesluiten, geen nadere betekenis kan toekomen. Daartoe acht het College met name van belang dat de publicatie – zo heeft de minister onbetwist gesteld – feitelijk handelen betreft. Het bestuursrecht biedt in beginsel geen rechtsbescherming tegen (de gevolgen) van dergelijk handelen. Voorgaande laat onverlet dat appellante de rechtmatigheid van de publicatie, alsmede haar vordering tot vergoeding van de door haar gestelde schade, kan voorleggen aan de burgerlijke rechter. Via die weg kan zij aldus gecompenseerd worden voor eventuele schade die zij lijdt ten gevolge van het beweerdelijk onrechtmatig feitelijk handelen, zodat ook in zoverre niet valt in te zien dat die schade aanleiding moet vormen om de hoogte van de boetes te verlagen.


















