Tweede evaluatie wet medisch-wetenschappelijk onderzoek met mensen
Hierbij bied ik u het rapport over de evaluatie van de Wet medisch-wetenschappelijk onderzoek met mensen (WMO) aan.1 Het is de tweede evaluatie van de wet sinds de inwerkingtreding in 1999.
In de eerste evaluatie van de WMO, waarvan het rapport eind 2004 is verschenen, is geconcludeerd dat de wet in het algemeen goed functioneert. Het belang van bescherming van de proefpersoon werd door alle betrokkenen gedragen, en kwam goed tot uitdrukking in de uitvoering van de wet. De door de onderzoekers gedane aanbevelingen om enkele knelpunten aan te pakken vormden mede aanleiding een wijziging van de wet voor te stellen.
Bij de nu uitgevoerde tweede evaluatie is gekozen de aandacht op vier specifieke punten te vestigen. Allereerst is aandacht gevraagd voor de ervaringen van proefpersonen bij deelname aan onderzoek, en de informatie die zij voorafgaand aan de deelname ontvangen. Ook is gevraagd te kijken naar de ervaringen van zowel onderzoekers als toetsingscommissies bij de uitvoering van de wet. Het derde onderdeel vormde de implementatie van de Europese Richtlijn voor de toetsing van klinisch geneesmiddelenonderzoek [red. Richtlijn 2001/20/EG]. Tot slot is gekeken naar de proefpersonenverzekering, zoals vastgelegd in de wet en het daarbij behorende Besluit verplichte verzekering bij medisch-wetenschappelijk onderzoek met mensen.
Het streven is in het najaar een kabinetsstandpunt op het evaluatierapport aan uw Kamer aan te bieden.
New EU rules for (active) medical devices utilising non-viable tissues of animal origin
Een bijdrage van Erik Vollebregt, Axon Lawyers.
 While everybody is starting up again after the summer and had 26 September as first major horizon date in their head (the date on which the Commission has said it will publish the proposed new EU medical devices rules), the EU decided to go ahead and change the rules for (active) medical devices utilising tissues of animal origin in a separate legal instrument, a Commission Regulation.
While everybody is starting up again after the summer and had 26 September as first major horizon date in their head (the date on which the Commission has said it will publish the proposed new EU medical devices rules), the EU decided to go ahead and change the rules for (active) medical devices utilising tissues of animal origin in a separate legal instrument, a Commission Regulation.
What is it about?
Commission Regulation 722/2012 concerning active implantable medical devices and medical devices manufactured utilising tissues of animal origin has just been published in the Official Journal of the European Union on 9 August 2012. It replaces the existing requirements contained in Directive 2003/32/EC and provides for procedures required when using tissues from TSE-susceptible animals in medical devices. The Regulation will apply from 29 August 2013. The obligation for Member States to verify that Notified Bodies have the up-to-date expertise to assess the conformity of medical devices in line with Regulation 722/2012) will enter into force on 29 August 2012. The Regulation did not come as a complete surprise (because a publicly available draft version had been shared with WTO members as part of the obligations in the Technical Barriers to Trade committee), although the timing of a Commission Regulation being final and published is always difficult to predict. Furthermore, why couldn’t this subject wait for inclusion in the new Regulation that is supposed to cover both active implantable and ‘other’ medical devices by merging Directives 90/285 and 93/42?
Any important changes?
Yes, at least some, although it is mostly merging of the Directive and the MEDDEV that currently deal with this subject. New is that the instrument is a regulation, which is a logical step in the process of the EU regulating more by directly applicable regulation in the life sciences industry rather than by directive, the latter leaving the Member States too much wiggle room for own interpretation. The new regulation expands the scope by including active implantable medical devices under Directive 90/385. It covers devices utilising tissues of animal origin (non-viable tissues and tissue derivatives originating from bovine, ovine and caprine species, deer, elk, mink and cats, to be precise) and links to Regulation 1069/2009 that provides for rules for sourcing of animal by-products not used for human consumption, as well as to Decision 2007/453 with respect to assessing the risk of the source country.
The general system set up under Directive 2003/32 stays the same (Annex I prescribing specific essential requirements for the devices concerned, some of which are updated and some of which are new), except that the procedure has been streamlined in a way that we may see under the new regulation for high risk medical devices in response to the ENVI complaints that I wrote about here and here. The regulation sets up a system for regulatory fast-tracking of summary evaluation reports regarding use of starting materials that have obtained a ‘TSE certificate of suitability’ from the European Directorate for the Quality of Medicines, based on the ‘coordinating Competent Authority’ model set out in section 6.0 of the MEDDEV. The Regulation provides for a model summary evaluation report in Annex II.
I have heard through the grapevine that the new general medical devices regulation may use a similar system, allowing Member States to comment on the Notified Body’s evaluation of high risk devices prior to CE marking, except if the evaluation shows that the device has been designed and evaluated in conformity with EU standards developed by a body to be appointed for this, perhaps SCENHIR that issued scientific reports on among other things reprocessing of devices in the past and which is now working on breast implant guidelines, or the JRC, the Commission’s inhouse scientific service.
Another important but not so new novelty in the Regulation is that the manufacturer has a positive obligation to collect, evaluate and submit to the Notified Body information regarding changes with regard to the animal tissue or derivatives used for the device or with regard to the TSE risk in relation to the device (a responsible manufacturer would do this already because this was already included in section 8.0 of the the non-binding MEDDEV). If the Notified Body subsequently concludes that such information leads to an increase of the overall TSE risk, the conformity of the device concerned must be assessed again, including the step of involving member states’ competent authorities.
Finally, the Regulation is more prescriptive in the evaluation required for renewal of a certificate by a Notified Body by setting out a minimum list of aspects to be evaluated by the Notified Body.
Of course among the points not discussed in this post there are other interesting details, like the new rigorous process for tallow derivates, copied straight from Annex I of the MEDDEV, so also not that new but now mandatory.
Why couldn’t this wait for the revision?
For two simple reasons, I think. First, it will take quite a while for the revision to trickle through the legislative process and enter into force (three years likely, with another year of transitional period). Second, Commissioner Dalli has in no uncertain terms requested member states to increase market surveillance for medical devices in early 2012. Out of all possible things the Commission does not need another PIP breast implant-like scandal to put another dent in the reputation of EU medical devices regulation, so it must have decided that devices utilising tissues of animal origin had sufficient potential in that respect to warrant regulating them ahead of schedule. Part of the market surveillance increase effort was an appeal to Member States to check if their Notified Bodies were still up to the task. A clear hint to this effect is made in recital 8 and article 4 (1), obliging the Member States to verify that the notified bodies designated to assess the conformity of medical devices manufactured utilising animal tissues have the necessary expertise and up-to-date knowledge to perform this task and to inform the Commission by 28 February 2013 of their findings. It is not excluded that the new revision Regulation will absorb this Commission Regulation by superseding it when it enters into force, so manufacturers should consider starting to plan for that to happen.
 With permission, CC-BY-SA medicaldeviceslegal.com.
With permission, CC-BY-SA medicaldeviceslegal.com.
Niet aannemelijk: binnen enkele weken zichtbaar resultaat
RCC 2 juli 2012, dossiernr. 2012/00482 (Nailner repair)
 Het betreft een tv-commercial voor het product Nailner Repair waarin zonder enige beperking wordt gezegd: "De Nailner formule dringt door het oppervlak van de nagel heen en geeft binnen enkele weken zichtbaar resultaat." Dat is bij klager niet het geval; zelfs na één jaar is er nog geen enkel resultaat.
Het betreft een tv-commercial voor het product Nailner Repair waarin zonder enige beperking wordt gezegd: "De Nailner formule dringt door het oppervlak van de nagel heen en geeft binnen enkele weken zichtbaar resultaat." Dat is bij klager niet het geval; zelfs na één jaar is er nog geen enkel resultaat.
Uit een e-mail van de Consumentenservice Nailner Repair begrijpt klager dat het product niet bij iedereen werkt. Dit dient uit de reclame te blijken. De KOAG/KAG heeft laten toevoegen dat de uitgroei van de teennagel 8 tot 12 maanden vergt. Het uiteindelijke resultaat van het gebruik van het product kan vanzelfsprekend van individu tot individu verschillen.
Omega distribueert het merk Nailner Repair voor het bedrijf YouMedical en de Commissie stelt voorop dat beide verweerders verantwoordelijk worden geacht voor de reclame. Medner heeft met een simpele verwijzing naar een studie (zonder toe te lichten op welke plaats verslag wordt gedaan, wat bedoeld wordt met positief resultaat en het aantal/percentage gebruikers bij wie in vier weken positief resultaat werd bereikt), niet aannemelijk gemaakt dat in het algemeen binnen enkele weken zichtbaar resultaat kan worden bereikt.
Klacht wordt deels gegrond verklaard vanwege strijd met 8.2 aanhef en onder b NRC jo. 7 NRC. In de uiting ligt niet de suggestie besloten dat een ieder onder alle omstandigheden baat zal vinden bij gebruik van het product.
3. Nu in de bestreden uiting zonder voorbehoud is gesteld: “De Nailner formule (…) geeft binnen enkele weken zichtbaar resultaat”, zonder dat verweerders aannemelijk hebben gemaakt dat in het algemeen een dergelijk resultaat kan worden bereikt, acht de Commissie de reclame voor de gemiddelde consument onduidelijk ten aanzien van de van het gebruik van Nailner Repair te verwachten resultaten als bedoeld in artikel 8.2 aanhef en onder b van de Nederlandse Reclame Code (NRC). Nu de gemiddelde consument er bovendien toe kan worden gebracht een besluit over een transactie te nemen, dat hij anders niet had genomen, is de uiting misleidend en daardoor oneerlijk in de zin van artikel 7 NRC.
4. Voor zover klager stelt dat uit de reclame dient te blijken dat het product niet bij iedereen werkt, wijst de Commissie de klacht af. In de uiting ligt niet de suggestie besloten dat een ieder onder alle omstandigheden baat zal vinden bij gebruik van het product.
Social media in relatie tot de Gedragscode Geneesmiddelenreclame
Stichting CGR, Social Media, Nieuwsbrief 2012-4.
 Uit de nieuwsbrief: Social media als Facebook. LinkedIn, twitter, blogs, discussiefora, Google en wiki zijn niet meer weg te denken in onze huidige manier van communiceren. En daarbij genieten de
Uit de nieuwsbrief: Social media als Facebook. LinkedIn, twitter, blogs, discussiefora, Google en wiki zijn niet meer weg te denken in onze huidige manier van communiceren. En daarbij genieten de
onderwerpen gezondheid, ziekten en behandelmethoden een grote populariteit.
Regelmatig worden ons vragen gesteld over social media in relatie tot de Gedragscode Geneesmiddelenreclame (hierna: de Gedragscode). De Gedragscode kent geen expliciete bepalingen over social media, maar is wel degelijk van toepassing, gezien de ruime definitie van reclame.
Hoofdregel is: wat “offline” geldt, geldt ook voor “online”. In deze nieuwsbrief zal nader worden ingegaan op de bijzondere kenmerken en toepassingen van social media in relatie tot de Gedragscode. Eventuele verplichtingen uit hoofde van de Wet bescherming persoonsgegevens of de Telecommunicatiewet, blijven buiten beschouwing.
De Gedragscode en social media
Voor social media geldt veelal dat het bereik niet bij de landsgrenzen ophoudt. De Gedragscode is alleen van
toepassing op uitingen die in Nederland toegankelijk zijn en wat woord en inhoud betreft, onmiskenbaar op het
Nederlandse publiek zijn gericht. Dit kan worden vastgesteld aan de hand van:
1. de taal waarin de uiting is gesteld;
2. de nationaliteit van de provider;
3. de vraag of en (zo ja) de wijze waarop de social media in nationale media wordt aangekondigd;
4. aanwezigheid van referenties aan het gebruik, de beschikbaarheid of de prijs van (bepaalde) geneesmiddelen in Nederland;
5. illustratieve aankleding en andere associaties met Nederland.
Het enkele feit dat het geneesmiddel ook in Nederland verkrijgbaar is, is niet doorslaggevend.
Algemene eisen die gelden voor social media:
1. Reclame moet altijd als zodanig herkenbaar zijn;
2. Herkenbaarheid van degene die de boodschap stuurt of (mede)verantwoordelijk is voor de inhoud daarvan;
3. Bepaalbaarheid van de geadresseerden (zie hieronder);
4. Verantwoordelijkheid voor de inhoud van eigen websites en media waarnaar wordt verwezen (gelinkt).
Bij het gebruik van social media is van belang dat het verbod op publieksreclame voor recept-geneesmiddelen in acht wordt genomen en publieksinformatie in overeenstemming is met de Leidraad informatie URgeneesmiddelen (hierna: de Leidraad). Dit betekent dat de geadresseerden goed moeten kunnen worden geïdentificeerd en geselecteerd. Social media kennen daar technische mogelijkheden voor door middel van preregistratie en/of gebruik van gebruikersnaam en
wachtwoord.
Verder is van belang dat informatie die door de farmaceutische onderneming via social media wordt verkregen over met name bijwerkingen van geneesmiddelen, worden opgevolgd binnen de geldende regels van farmacovigilantie.
Uitleg van het begrip 'Informed consent'
Rechtbank Rotterdam 18 april 2012, LJN BW4629 (eiser tegen Stichting Franciscus Gasthuis)
L etselschade, aansprakelijkheid, medische behandeling, informed consent, medische fout, , dilatatietherapie. Dit vonnis spreekt over een uitgebreide uiteenzetting van de 'informed consent' voorafgaand aan een operatieve ingreep en behandeling van een complicatie. De zaak wordt aangehouden, want er wordt een deskundige aangewezen.
etselschade, aansprakelijkheid, medische behandeling, informed consent, medische fout, , dilatatietherapie. Dit vonnis spreekt over een uitgebreide uiteenzetting van de 'informed consent' voorafgaand aan een operatieve ingreep en behandeling van een complicatie. De zaak wordt aangehouden, want er wordt een deskundige aangewezen.
Informed consent
Op de hulpverlener rust een informatieplicht. De hulpverlener licht de patiënt op duidelijke wijze, en desgevraagd schriftelijk in over het voorgenomen onderzoek en de voorgestelde behandeling en over de ontwikkelingen omtrent het onderzoek, de behandeling en de gezondheidstoestand van de patiënt (artikel 7:448, lid 1, BW). Bij het uitvoeren van voornoemde verplichting laat de hulpverlener zich leiden door hetgeen de patiënt redelijkerwijze dient te weten ten aanzien van:
a. de aard en het doel van het onderzoek of de behandeling die hij noodzakelijk acht en van de uit te voeren verrichtingen;
b. de te verwachten gevolgen en risico's daarvan voor de gezondheid van de patiënt;
c. andere methoden van onderzoek of behandeling die in aanmerking komen;
d. de staat van en de vooruitzichten met betrekking tot diens gezondheid voor wat betreft het terrein van het onderzoek of de behandeling (artikel 7:448, lid 2, BW).
(...)
Een hulpverlener kan zich in beginsel slechts op door de patiënt verleende toestemming beroepen indien die patiënt voorafgaande aan het verlenen van toestemming naar behoren was geïnformeerd. Wat in dit verband "naar behoren informeren" inhoudt, is afhankelijk van de concrete omstandigheden van het geval. Daarbij kunnen aspecten aan de orde zijn als:
- Bestaan er voor patiënt reële keuzemogelijkheden. Dat is bijvoorbeeld het geval indien de patiënt zonder het risico op gezondheidsschade kan besluiten een behandeling niet te ondergaan, of te kiezen voor een andere behandeling. Des te reëler de keuzemogelijkheden van de patiënt zijn des te belangrijker is het dat de patiënt goed over de verschillende alternatieven en de daaraan verbonden voor- en nadelen wordt geïnformeerd.
- Hoe groot zijn de aan een behandeling verbonden risico's en hoe ernstig kunnen de gevolgen zijn indien zich een dergelijk risico realiseert. Des te groter de risico's en des te ernstiger de mogelijke gevolgen, des te beter de patiënt daarover zal dienen te worden geïnformeerd.
- Welke informatie wenst de patiënt te verkrijgen en in welke mate is de patiënt in staat om die informatie te begrijpen en mede op basis daarvan keuzes te maken. Naarmate een patiënt en de zijnen minder behoefte hebben aan uitgebreide informatie en minder in staat zijn om de informatie te begrijpen en om mede op basis daarvan keuzes te maken omtrent de behandeling, ligt het in de rede dat de te verstrekken informatie minder gedetailleerd zal behoeven te zijn.
- Bestaat er binnen de beroepsgroep consensus over de informatie die in een bepaald geval behoort te worden verstrekt. Indien dit het geval is, hetgeen bijvoorbeeld tot uitdrukking kan komen in patiëntenbrochures, dan ligt het in de rede dat in ieder geval die informatie zal worden verstrekt.
Informed consent - operatieve ingreep
(...) Of [eiser] er over had behoren te worden geïnformeerd dat de slikklachten zo ernstig zouden kunnen zijn als in de praktijk is gebleken, is (mede) afhankelijk van de grootte van het risico op dergelijk ernstige slikklachten, de mogelijkheden om die vervolgens te verhelpen en de daaraan verbonden risico's, alsmede van de ernst van het gezondheidsprobleem dat men beoogde met de ingreep van 15 juli 2004 te verhelpen en de beschikbare alternatieven voor de voorgestelde ingreep.
Uit de stellingen van [eiser] en hetgeen zij ter zitting heeft opgemerkt, kan worden opgemaakt dat zij heeft bedoeld te stellen dat zij geen toestemming voor de operatie zou hebben verleend indien zij volledig zou zijn geïnformeerd.
Informed consent - behandeling complicatie
De stelling van Sint Franciscus Gasthuis dat "de hoop en verwachting bestond" dat de na de operatie gebleken problemen met behulp van de dilataties konden worden opgelost, kan de rechtbank niet rijmen met de erkenning van [X] ter zitting dat het percentage patiënten dat baat heeft bij dilatatietherapie - naar de rechtbank aanneemt in een geval als het onderhavige - kleiner is dan 20%. Bij een succeskans van minder dan 20% was immers geen sprake van een reële verwachting dat de problemen met behulp van de dilataties zouden kunnen worden opgelost.
Beoordeeld dient te worden of redelijk bekwaam en redelijk handelend vakgenoten van [X] en [Y] in de gegeven omstandigheden dilatatietherapie zouden hebben geadviseerd in plaats van re-operatie, alsmede of aannemelijk is dat een patiënt voor dilatatietietherapie zou hebben gekozen na adequate voorlichting. Teneinde dit te kunnen beoordelen dient meer inzicht te worden verkregen in de mogelijkheden, kansen en risico's.(...)
Deskundige
Uit hetgeen hiervoor is overwogen, vloeit voort dat de rechtbank het noodzakelijk acht zich te laten adviseren door een onafhankelijk deskundige. Weliswaar is reeds een advies van een deskundige beschikbaar in de vorm van de door [eiser] overgelegde brief van [Z], maar de aan [Z] voorgelegde vragen - welke niet aan de rechtbank bekend zijn gemaakt - hebben kennelijk niet alle hiervoor genoemde door de rechtbank relevant geachte aspecten omvat. Bovendien is het advies niet uitgebracht op gezamenlijk verzoek van partijen op basis van een gezamenlijke vraagstelling en door een in overleg tussen (de medisch adviseurs van partijen) gekozen deskundige. Daarmee is de processuele waarde van het advies van [Z] ook beperkt.
Testimonial van een "gewone" consument
RCC 24 juli 2012, dossiernr. 2012/00551 (Brandend maagzuur? Renate weet raad)
 In een weekblad staan advertorials waarin Rennie en Losecosan worden aangeprezen door Renate (een moeder van drie kinderen en schooljuf)
In een weekblad staan advertorials waarin Rennie en Losecosan worden aangeprezen door Renate (een moeder van drie kinderen en schooljuf)
Klacht: Er wordt advies gegeven over het gebruik van maagzuurremmende middelen, dit mag uitsluitend door een professional of gediplomeerde drogist/apotheker worden gedaan (strijd met 8,9,10,15,16,17,18,20,24,25 Code Publieksreclame voor Geneesmiddelen).
Het verweer dat een testimonial van een "gewone" consument mag en de KOAG/KAG heeft de uiting goedgekeurd en van een toelatingsnummer voorzien wordt door KOAG/KAG ondersteund. De klacht wordt afgewezen.
KOAG/KAG: In de advertorials is sprake van een aanbeveling van een "gewone" consument en niet van een aanbeveling door een beroepsbeoefenaar, wetenschapper of persoon met een zekere reputatie op het gebied van geneesmiddelen, wat volgens artikel 19 van de Bijzondere Reclamecode CPG niet is toegestaan. De advertorials voldoen aan de geldende wet- en regelgeving in het algemeen en de CPG in het bijzonder.
De Commissie vat klaagsters voornaamste bezwaar tegen de onderhavige - door de KOAG goedgekeurde - reclame-uitingen aldus op, dat sprake is van een aanbeveling van maagzuurremmende middelen door iemand die daartoe niet gekwalificeerd is. Op grond van artikel 19 CPG mag reclame echter niet direct of indirect een aanprijzing bevatten van wetenschapsbeoefenaren of beroepsbeoefenaren in de gezondheidszorg, waartoe de volgens klaagster wel gekwalificeerde “professional” en “gediplomeerd drogist/apotheker” gerekend moeten worden. Niet kan worden geoordeeld dat “Renate” door haar beroep van onderwijzeres op een basisschool gezag geniet op het gebied van geneesmiddelen en om die reden - op basis van artikel 19 CPG - niet de producten Rennie en Losecosan 20 zou mogen aanprijzen.
Van strijd met de overige door klaagster aangehaalde artikelen uit de CPG is de Commissie evenmin gebleken.
Niet iedere werkingsfase in beeld gebracht
Vz. (afwijzing) RCC 7 maart 2012, dossiernr. 2012/00163 (Bisolvon in de longen)
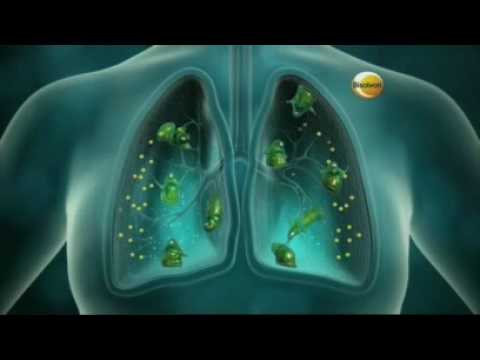 In een televisiereclame wordt door middel van een schematische weergaven van de borst toegelicht hoe Bisolvon werkt.
In een televisiereclame wordt door middel van een schematische weergaven van de borst toegelicht hoe Bisolvon werkt.
In de animatie die in de uitingen wordt getoond is te zien dat Bisolvon wordt gedronken, waarna dit het vastzittende slijm in de luchtwegen oplost. Klacht: Wat men eet en drinkt komt echter in de slokdarm en niet in de luchtweg. Ten onrechte wordt de indruk gewekt dat Bisolvon, na het drinken daarvan, in de longen terechtkomt. De uiting is om die reden misleidend.
De voorzitter wijst de klacht af en overweegt dat de korte animatiebeelden op een versimpelde wijze de werking uitlegt: het innemen en de laatste fase, het moment dat Bisolvon zijn werk doet, wordt in beeldgebracht zonder tussenliggende fase te tonen.
De voorzitter is van oordeel dat de klacht de Commissie geen aanleiding zal geven een aanbeveling te doen. Hij overweegt daartoe het volgende.
Door middel van enkele korte animatie-beelden wordt op versimpelde wijze getoond wat in de uiting over de werking van Bisolvon wordt gezegd, in die zin dat de eerste, het innemen van Bisolvon, en de laatste fase, het moment waarop Bisolvon in de longen zijn werk doet, in beeld worden gebracht. Dat niet iedere fase die Bisolvon doorloopt wordt getoond, leidt niet tot het oordeel dat de uitingen misleidend zijn.
QR-code hulpmiddel, maar geen oplossing voor bestrijding namaakmedicijnen
 Een bijdrage van Corina Post-Wolfert, Abcor Merkenbureau.
Een bijdrage van Corina Post-Wolfert, Abcor Merkenbureau.
Eerder gepubliceerd in het Noordhollands Dagblad. Snel geld verdienen wil iedereen wel. Over het algemeen moet je hiervoor hard werken of geluk hebben in de loterij. Ben je creatief dan kan een uitvinding tot succes leiden. Er zijn dan altijd anderen die graag willen aanhaken aan dit success en dit gebeurd dan niet altijd eerlijk. Het product wordt nagemaakt en het merk van de ander wordt er opgezet. We kennen allemaal de op grote schaal nagemaakte kleding (Adidas), schoenen (Convers), tassen (Louis Vuiton), parfums (Chanel), toiletartikelen (Gilette) etc. Door de opkomst van het electronische dataverkeer is het bestrijden van de nepartikelen een lastige strijd geworden.
Het verbieden van de website van een aanbieder van nep-producten (counterfeiter) is weinig effectief. De counterfeiter zal via een andere website zijn producten blijven aanbieden. De creativeit van een counterfeiter is ook toegenomen. Via blurring maken zij het uiterlijke van een verpakking wazig zodat het onduidelijk is dat het om een merkproduct gaat. Of bij een zoekopdracht is het niet gelijk duidelijk wie een merkproduct aanbied. Verschillende velden moeten hiervoor namelijk open geklikt worden om hier achter te komen.
De houder van het merkartikel loopt door productvervalsing vele miljoenen aan inkomsten mis. De consument ondervindt enige hinder wanneer het nep-product van slechte kwaliteit is. Het is echter levensbedreigend wanneer het om een medicijn gaat dat niet of te weinig van de werkzame stof bevat. Medicijnvervalsing is een wereldwijd probleem dat in raptempo toeneemt. De counterfeiters zijn vaak goed georganiseerde maffiabendes die hun terrein verlegd hebben van de (party)drugs naar medicijnen. De winst is hoog, de pakkans is klein en de straffen zijn laag.
De meeste medicijnen die worden nagemaakt zijn lifestyle medicijnen tegen bijvoorbeeld allergie (ALLERFREE), erectiestoornis (VIAGRA) of depressies ( SEROQUEL). Deze medicijnen worden voornamelijk aangeboden in welvarende landen. In de ontwikkelingslanden worden medicijnen nagemaakt die een life-threatening conditie hebben, te denken valt aan: malaria, tuberculosis en HIV/AIDS. Door de jaren heen worden ook de dure anti-kanker medicijnen nagemaakt en de populaire anti-virale medicijnen. Om hoeveel medicijnvervalsing het per jaar gaat, is niet precies bekend. De World Health Organisatie (WHO) schat dat de helft van de medicijnen die aangeboden worden op het internet nep zijn.
Het is soms lastig om nep van echt te onderscheiden. Dit komt omdat de machines van de counterfeiters van de nieuwste kwaliteit zijn waardoor de nep-medicijnen er vaak bijzonder goed uitzien. Pas als het medicijnen onder de loep wordt gelegd, blijkt dat het een andere samenstelling te hebben. Uit onderzoek blijkt bijvoorbeeld dat malariatabletten te weinig Arthemisine bevatten waardoor bij gebruik de malariamug niet dood gaat maar juist resistent wordt door het gebruik van het medicijn. Anti-kanker medicijnen kunnen zuren of rattengif bevatten om de patient te laten denken dat het medicijn werkt omdat zij misselijk worden. In werkelijkheid worden zij nog zieker gemaakt. In andere gevallen blijken de medicijnen perfect nagemaakt te zijn. Laboratorium onderzoek moet dan uitwijzen of de gebruikte actieve stoffen anders zijn dan het origineel. Op het internet is het niet te zien dat het om het echte medicijn gaat. Bij het aanbieden van nepmedicijnen op een website zal de inbreukmakende producent er alles aan doen om de verpakking er zo goed mogelijk uit te laten zien om de koper de indruk te geven dat het om het originele product gaat.
De gevolgen van counterfeit strekken zich niet alleen uit tot de patient maar ook tot de farmaceutische industrie zelf. In vergelijkende studies met een comparator moet de industrie bij de aankoop van het vergelijkende medicijn ook uitkijken dat zij niet namaak producten gaat gebruiken. Een studie is dan “at risk” omdat de gegevens niet meer kloppen. Tevens loopt de proefpersonen in de klinische studie een mogelijk gevaar wanneer zij een namaakmedicijn toegediend krijgen. De industrie doet er daarom goed aan om het comparator medicijn af te nemen van de reguliere groothandel.
De Federation of Pharmaceutical Industries and Association (EFPIA) is in ver gevorderd overleg met de Europese Commissie (EC) over het aanpakken van nep-medicijnen. Het voorstel is om een centraal tracking-systeem in te voeren voor medicijnen. De verpakking krijgt dan een QR-code. In Frankrijk is een QR-code al verplicht voor medicijnverpakkingen. Het Nederlands Verpakkingscentrum (NCV) heeft voorgesteld om er een unieke code van te maken. Deze matrixcode staat voor een uniek cijfer dat gelinkt is aan de historie van het medicijn dat wordt bijgehouden in een centraal databestand. Door de code voor een mobiele telefoon of scanapparaat te houden, wordt er een verbinding gemaakt met het centrale websysteem. De apotheker of de patient controleert vervolgens of het medicijn van de orginele eigenaar afkomstig is. Daarnaast worden op de verpakkingen speciale stickers/sluitingen aangebracht. Deze stickers bestaan uit vezels zodat bij misbruik vezelsporen achterblijven op de verpakking.
De EC wil graag een tracking systeem invoeren dat de gehele route van het medicijn volgt. Dus vanaf het begin van de grondstoffen die gebruikt worden, het verwerken tot een medicijn en uiteindelijk het aanleveren aan de distributeur (apotheek, ziekenhuis, etc). Dit systeem is duur. Daarom pleit de EFPIA voor een alternatief, namelijk een systeem dat het medicijn vanaf de fabrikant tot aan de distributeur bijhoudt. Bovendien wil de vakorganisatie dat deze verpakkingsrichtlijn alleen voor de innovatieve medicijnen (dus medicijnen die nog onder een octrooi vallen) gaat gelden.
EFPIA vreest dat de invoering van een nieuwe verpakkingsrichtlijn leidt tot stagnatie bij de productie van de huidige medicijnen. De dossiers van bestaande medicijnen moeten mogelijk opnieuw gekeurd worden door de gezondheidsautoriteiten omdat de verpakking aangepast worden aan de nieuwe richtlijnen. Dit kan vertraging van de productie tot gevolg hebben. In het ergste geval zou een bestaand product van de markt gehaald worden omdat de klinische studies van toen niet meer voldoen aan de huidige normen. Nieuwe klinische studies zijn dan noodzakelijk. Deze extra studies en het niet op de markt mogen brengen van het medicijn is een grote kostenpost voor de industrie en zal medicijntekorten in de hand werken bij consumenten. Daarom wil de industrie het nieuwe systeem alleen invoeren voor nieuwe innovatieve producten wil en niet voor bestaande producten waar geen octrooi meer voor geldt.
Het zal daarom nog de nodige discussies met zich meebrengen voordat alle neuzen in dezelfde richting staan om een unieke QR code in te voeren. Naast deze voorgenomen plannen is er ook een nieuwe wet opgesteld, de Anti-Counterfeiting Trade Agreement (ACTA). Maar ook de goedkeuring en implementatie van dit instrument om counterfeit te lijf te gaan, verloopt niet zonder slag of stoot. De Europese Commissie heeft onlangs deze wet afgekeurd en het Europees parlement zal dit advies hoogstwaarschijnlijk volgen. De wet is namelijk conflicterend met een aantal Europese regels. Daarnaast is men ook nog bezig aan de harmonisatie van bestaande nationale richtlijnen om deze aan te passen aan de Europese richtlijnen. Het heeft dus heel veel voeten in de aarde om een centraal trackingsysteem in te voeren en de wetten geharmoniseerd dan wel een nieuwe anti-counterfeitwet te krijgen om namaak producten tegen tegaan.
Als alternatief wordt er een ander instrument ingeschakeld namelijk het creëren van een grotere bewustwording onder het publiek. De reguliere bevolking moet inzicht krijgen in de gevaren van het aanschaffen van medicijnen via het internet. Douane beambten, autoriteiten, apothekers en medisch specialisten moeten onderwezen worden over de kwaliteit van het product. In Nederland is, voor zover men weet, de reguliere supply chain nog niet besmet met counterfeit producten.
De QR- code waarborgt de toevoer van geneesmiddelen beter maar daarnaast moet men zich blijven richten tot het reguliere kanaal en niet het internet zodat de counterfeiter zijn nepmedicijn moeilijk zal slijten. Veel maatregelen worden genomen om de volkgezondheid te waarborgen. Alleen de grote vraag is wie de kosten van al deze maatregelen gaat dragen. Het laatste woord is hier nog niet over gezegd.
Corina Post-Wolfert, Abcor Merkenbureau
Beschikbaarheid van geneesmiddelen is belang van het Land
Gerecht in eerste aanleg van Curaçao 4 juli 2012, LJN BX4886 (Vereniging van importeurs van pharmaceutische produkten [VIPP] tegen Het Land Curaçao)
 In geschil is de invoering van maximum prijzen voor geneesmiddelen. Bij Ministeriële Regeling met Algemene Werking van 8 mei 2012, ter uitvoering van artikel 2 van de Prijzenverordening, zijn de per 1 juli 2012 geldende prijzen voor het door importeurs op Curaçao aanbieden of verkopen van geneesmiddelen aan een maximum gebonden. (P.B. Ao 2012 No 28 - Regeling maximumprijzen geneesmiddelen juli 2012).
In geschil is de invoering van maximum prijzen voor geneesmiddelen. Bij Ministeriële Regeling met Algemene Werking van 8 mei 2012, ter uitvoering van artikel 2 van de Prijzenverordening, zijn de per 1 juli 2012 geldende prijzen voor het door importeurs op Curaçao aanbieden of verkopen van geneesmiddelen aan een maximum gebonden. (P.B. Ao 2012 No 28 - Regeling maximumprijzen geneesmiddelen juli 2012).
De VIPP heeft gesteld dat de beschikbaarheid van geneesmiddelen als gevolg van de Regeling niet meer gewaarborgd zal zijn. Het Gerecht oordeelt dat de beschikbaarheid van geneesmiddelen de verantwoordelijkheid is van het Land en niet een belang dat de VIPP volgens haar statuten behartigt. De regering heeft toegezegd de ingangsdatum te willen opschorten tot 1 september. Het Gerecht wijst de gevraagde voorzieningen van de VIPP af.
15. De beschikbaarheid van geneesmiddelen op Curaçao is geen belang dat de VIPP volgens haar statuten behartigt. Het is de verantwoordelijkheid van het Land, dat die verantwoordelijkheid ook zegt te nemen. In het kader van dit kort geding kan daarop dan ook niet verder worden ingegaan. Van de zijde van het Land is ter zitting aangedrongen op goede communicatie met de VIPP. Daaraan zou het hebben ontbroken, nadat de VIPP geen gehoor vond voor haar bezwaren tegen de voorgenomen Regeling. Voor een behoorlijke uitvoering van de Regeling lijkt een goede communicatie tussen de VIPP en de betrokken afdeling van het Land inderdaad van groot belang. Daarbij behoort ook een goede informatievoorziening over en weer, waarmee inmiddels (weer) een begin is gemaakt door toezending van de gegevens die aan bijlage I ten grondslag hebben gelegen. Mogelijke knelpunten zullen immers in een zo vroeg mogelijk stadium moeten worden opgespoord om stagnatie in de geneesmiddelenvoorziening te voorkomen. Artikel 4 van de Regeling biedt ten slotte de mogelijkheid om deze ook vaker dan tweemaal per jaar te wijzigen.
16. De slotsom is dat, met inachtneming van de hiervoor onder 6. weergegeven criteria, voorshands niet kan worden gezegd dat de Regeling onmiskenbaar onverbindend is. De gevraagde voorziening zal dan ook worden geweigerd, met verwijzing van de VIPP als de in het ongelijk gestelde partij in de proceskosten, die aan de zijde van het Land worden begroot op Naf. 1.500,00 wegens salaris van de gemachtigde.
Gevoelens van angst voor bijwerkingen
RCC 22 februari 2012, dossiernr. 2011/01208 (Remark groep Appeleren aan gevoelens van angst voor bijwerkingen geneesmiddelen; misleiding)
 In een serie uitingen over geneesmiddelen is onder andere opgenomen: onder A. “Grijp niet direct naar een geneesmiddel als je ergens last van hebt. Ga niet direct iets slikken bij elk ongemak. Zeker als je probleem redelijk aan de buitenkant van je lichaam zit. Dan is het logischer en efficiënter een middel te gebruiken dat ter plekke zijn werk doet. Dat is minder belastend voor je lichaam. Zo voorkom je nare bijwerkingen. En het levert vaak betere resultaten.” Klager meent dat de tekst appelleert aan angstgevoelens, ex artikel 6 NRC, dat er sprake is van agressieve reclame en dat er op een denigrerend wijze gesproken wordt over geneesmiddelen. Tot slot zijn de I SAY-producten slechts hulpmiddelen, die niet door het CBG worden beoordeeld en de mededeling "vaak betere resultaten" is daarom misleidend ex artikel 8 NRC. In een uitgebreid oordeel worden de klachten voor het overgrote deel gegrond verklaard en een aanbeveling gedaan.
In een serie uitingen over geneesmiddelen is onder andere opgenomen: onder A. “Grijp niet direct naar een geneesmiddel als je ergens last van hebt. Ga niet direct iets slikken bij elk ongemak. Zeker als je probleem redelijk aan de buitenkant van je lichaam zit. Dan is het logischer en efficiënter een middel te gebruiken dat ter plekke zijn werk doet. Dat is minder belastend voor je lichaam. Zo voorkom je nare bijwerkingen. En het levert vaak betere resultaten.” Klager meent dat de tekst appelleert aan angstgevoelens, ex artikel 6 NRC, dat er sprake is van agressieve reclame en dat er op een denigrerend wijze gesproken wordt over geneesmiddelen. Tot slot zijn de I SAY-producten slechts hulpmiddelen, die niet door het CBG worden beoordeeld en de mededeling "vaak betere resultaten" is daarom misleidend ex artikel 8 NRC. In een uitgebreid oordeel worden de klachten voor het overgrote deel gegrond verklaard en een aanbeveling gedaan.
1. Tussen partijen is niet in geschil dat de producten waarop de bestreden uitingen betrekking hebben medische hulpmiddelen zijn in de zin van artikel 1 van de Wet op de medische hulpmiddelen (WMH). In reactie op de klacht is namens adverteerder aangevoerd dat de
i say producten een CE-markering met nummeraanduiding hebben. Het is de Commissie bekend dat een dergelijke CE-markering krachtens artikel 7 van het Besluit medische hulpmiddelen (BMH) wordt afgegeven door een aangewezen instantie die heeft geverifieerd of sprake is van conformiteit van het betreffende product met de essentiële eisen die op het product van toepassing zijn. Nu door Bayer echter niet wordt betwist dat de i say producten een CE-markering hebben, maar - kort samengevat - wordt gesteld dat de uitingen misleidend zijn en appelleren aan gevoelens van angst, kan de verleende CE-markering in de verdere beoordeling buiten beschouwing blijven.
2. Met betrekking tot het beroep van Bayer op artikel 6 NRC overweegt de Commissie het volgende.
Met de tekst “Grijp niet direct naar een geneesmiddel als je ergens last van hebt. Ga niet direct iets slikken bij elk ongemak. Zeker als je probleem redelijk aan de buitenkant van je lichaam zit. Dan is het logischer en efficiënter een middel te gebruiken dat ter plekke zijn werk doet. Dat is minder belastend voor je lichaam. Zo voorkom je nare bijwerkingen. En het levert vaak betere resultaten.” wordt naar het oordeel van de Commissie ingespeeld op gevoelens van angst voor “nare bijwerkingen” van geneesmiddelen. Hiervoor bestaat geen aanleiding. Daarom acht de Commissie de hiervoor aangehaalde tekst op de verpakkingen en de website in strijd met artikel 6 NRC, waarin is bepaald dat reclame zonder te rechtvaardigen redenen niet mag appelleren aan gevoelens van angst.
3. Naar het oordeel van de Commissie is tevens sprake van misleidende reclame. Van de naam “i say bye-bye..” in combinatie met het noemen van een kwaal gaat de suggestie uit dat de kwaal waarvoor het product bestemd is geheel weggaat. In de onder A t/m C aangehaalde uitingen wordt gesteld dat het gebruik van de i say producten logischer en efficiënter is dan het gebruik van geneesmiddelen, de i say producten minder belastend zijn voor het lichaam en de resultaten vaak beter zijn dan bij geneesmiddelen. Voorts wordt geclaimd dat de i say producten geen bijwerkingen kennen en “volkomen veilig” zijn. Nu deze stellingen door Bayer gemotiveerd zijn aangevochten, ligt het op de weg van adverteerder de juistheid ervan aannemelijk te maken. Naar het oordeel van de Commissie is adverteerder daarin niet geslaagd. Ten aanzien van deze kwalificaties is immers geen inhoudelijk verweer gevoerd.
Gelet op het vorenstaande gaan de uitingen gepaard met onjuiste informatie ten aanzien van de voordelen van de i say producten als bedoeld in artikel 8.2. aanhef en onder b NRC. Omdat de Commissie voorts van oordeel is dat de gemiddelde consument door de uitingen ertoe gebracht kan worden een besluit over een transactie te nemen dat hij anders niet had genomen, zijn de uitingen misleidend en daardoor oneerlijk in de zin van artikel 7 NRC.
4. Van agressieve reclame in de zin van artikel 14 lid 1 NRC is sprake als reclame door intimidatie, dwang, inclusief het gebruik van lichamelijk geweld, of ongepaste beïnvloeding de keuzevrijheid of de vrijheid van handelen van de gemiddelde consument met betrekking tot het product aanzienlijk beperkt of kan beperken. Blijkens de toelichting bij artikel 14 NRC wordt onder ongepaste beïnvloeding verstaan het uitbuiten van een machtspositie ten aanzien van de consument om pressie uit te oefenen op een wijze die het vermogen van de consument om een geïnformeerd besluit te nemen, aanzienlijk beperkt. Een dergelijke situatie doet zich naar het oordeel van de Commissie in het onderhavige geval niet voor, zodat de klacht dat sprake is van agressieve en om die reden oneerlijke reclame in de zin van artikel 7 NRC wordt afgewezen.



















