Jurisprudentielunch Reclamerecht 2013


Op donderdag 30 mei van 12.00 – 15.15 organiseert eduLex, onderdeel van deLex, wederom een jurisprudentiebijeenkomst over reclamerecht in De Balie te Amsterdam. Tijdens deze bijeenkomst behandelen twee ervaren sprekers (Ebba Hoogenraad en professor Jan Kabel) belangrijke en actuele jurisprudentie. Zowel Nederlandse uitspraken, zelfregulering en Europese uitspraken rondom commerciële communicatie komen aan bod. Het gaat onder meer over vergelijkende reclame in de gewone rechtspraak over de laatste tien jaar (na de implementatie in april 2002 van Richtlijn 97/55/EG).
Ook komen de ontwikkelingen op het gebied van het ‘reclame’-begrip, misleiding, kleine lettertjes, autoreclames aan bod.
11.30 – 12.00 uur Ontvangst en intekenen
12.00 – 13.30 uur prof. Jan Kabel, IViR en DLA Piper
13.45 – 15.15 uur Ebba Hoogenraad, Hoogenraad & Haak
15.15 uur Einde programma
Locatie
De Balie, Kleine Gartmanplantsoen 10, Amsterdam (route plannen, parkeersuggestie).
Datum/ Tijd
Donderdag 30 mei 2013, 12u00 - 15u15.
Kosten deelname
€ 325,00 Per persoon
€ 285,00 Sponsors Reclameboek/leden VvRr, en
€ 95,00 Rechterlijke macht/wetenschappelijk personeel (full time)
Genoemde prijzen zijn incl. lunch, koffie, thee, documentatie, excl. BTW.
Kosten voor het herontwerpen laboratorium
Rechtbank Almelo 8 augustus 2012, LJN BX6857 (PANalytical B.V. tegen gedaagde)
 Met samenvatting van Robert Kreuger, masterstudent Internet, IE en ICT VU Amsterdam
Met samenvatting van Robert Kreuger, masterstudent Internet, IE en ICT VU Amsterdam
Vervolg op IT 683 ‘Bouw van een nieuw geautomatiseerd laboratorium’. Overeenkomst met betrekking tot de bouw en realisatie van een nieuw geautomatiseerd laboratorium. Schadeberekening. De kosten verbonden aan het "herontwerpen" van het Systeem komen voor vergoeding in aanmerking. PANalytical kan onderbouwen dat het ging om "hardware for upgrade of send and receive station".
Door een nadere uitleg van PANalytical betreffende de facturen van materialen van Metal B.V. zijn de kosten van het herontwerpen voldoende onderbouwd. Er is aannemelijk gemaakt dat die materialen inderdaad nodig waren met het oog op bedoeld herontwerpen. Ook heeft PANalytical door overlegging van de opdrachtbevestiging van TKS voldoende aannemelijk gemaakt dat door haar met TKS de daarin genoemde betalingstermijnen waren overeengekomen en TKS deze op latere tijdstippen dan overeengekomen heeft betaald. De rechtbank zal bij de bepaling van de schade uitgaan van een renteverlies, hetgeen ook geldt voor de te late betaling van de – contractueel overeengekomen – boete.
De schade die PANalytical lijdt is alle vermogensschade - voorzover door de rechtbank toegewezen - die is veroorzaakt door [gedaagde]s wanprestatie en door de (gedeeltelijke) ontbinding als gevolg daarvan. Er is geen aanleiding of rechtsgrond een "besparing" van PANalytical, in de vorm van een niet te betalen deel van de aanneemsom in mindering te brengen op het schadebedrag.
3.12 [gedaagde] miskent hiermee echter dat de schade die PANalytical lijdt alle vermogensschade - voorzover door de rechtbank toegewezen - is die is veroorzaakt door [gedaagde]s wanprestatie en door de (gedeeltelijke) ontbinding als gevolg daarvan. Er is geen aanleiding of rechtsgrond een "besparing" van PANalytical, in de vorm van een niet te betalen deel van de aanneemsom in mindering te brengen op het schadebedrag. Als gevolg van de gedeeltelijke ontbinding van de overeenkomst is er ook geen grond om bij de bepaling van de schade rekening te houden met vergoedingen van werk ten behoeve van "aanvullende wensen van PANalytical", nog daargelaten dat hetgeen [gedaagde] daarover heeft gesteld onvoldoende specifiek is en door PANalytical gemotiveerd is betwist.
3.13 Op basis van o.a. de kosten van het herontwerpen en het geleden renteverlies, alsook hetgeen reeds in het Tussenvonnis (LJN: BV6074) is overwogen, komt de rechtbank tot de volgende schadeberekening:
(i) kosten herontwerpen € 115.518,--
(ii) extra arbeidsuren € 71.325,--
(iii) reis- en verblijfskosten € 16.000,--
(iv) extra managementstijd € 0,--
(v) renteverlies € 111.164,--
(vi) boete TKS € 165.750,--
(vii) extra manuren etc. klant Frankrijk € 0,--
Totaal € 479.757,--
Tijdelijke karakter activiteiten niet relevant
College van Beroep voor het Bedrijfsleven 2 april 2013, LJN BZ8258 (Eureka tegen Minister) Rechtspraak.nl: Boete wegens overtreding artikel 11 in verbinding met artikel 10 van de Tabakswet, in verbinding met artikel 3, tweede lid, aanhef en onder b en/of c, van het Besluit beperking verkoop en gebruik tabaksprodukten. Naar het oordeel van het College heeft de rechtbank ten onrechte overwogen dat in dit geval geen sprake is van een inrichting waarin voorzieningen worden aangeboden op de terreinen van maatschappelijke ondersteuning en een inrichting voor kunst en cultuur. Op de beheerder van de inrichting rust de verplichting maatregelen te treffen ter voorkoming van hinder en overlast van roken, waaronder ten minste het instellen, aanduiden en handhaven van een rookverbod als bedoeld in artikel 10 van de Tabakswet.
Rechtspraak.nl: Boete wegens overtreding artikel 11 in verbinding met artikel 10 van de Tabakswet, in verbinding met artikel 3, tweede lid, aanhef en onder b en/of c, van het Besluit beperking verkoop en gebruik tabaksprodukten. Naar het oordeel van het College heeft de rechtbank ten onrechte overwogen dat in dit geval geen sprake is van een inrichting waarin voorzieningen worden aangeboden op de terreinen van maatschappelijke ondersteuning en een inrichting voor kunst en cultuur. Op de beheerder van de inrichting rust de verplichting maatregelen te treffen ter voorkoming van hinder en overlast van roken, waaronder ten minste het instellen, aanduiden en handhaven van een rookverbod als bedoeld in artikel 10 van de Tabakswet.
Met samenvatting van Robert Kreuger, masterstudent Internet, IE en ICT VU Amsterdam.
Voor de vraag of een inrichting voor maatschappelijke ondersteuning en/of kunst en cultuur onder het ‘Besluit beperking verkoop en gebruik tabaksprodukten’ valt is beslissend dat door de inrichting feitelijk voorzieningen worden aangeboden op het terrein van de bevordering van de sociale samenhang in en de leefbaarheid van dorpen, wijken en buurten. Een tijdelijk karakter van de voorzieningen doet hier niet aan af.
Eureka is een sociaal-culturele vereniging gevestigd in Zwolle. De minister heeft bij besluit van 3 april 2009, kenmerk 200900883, aan Eureka een boete van € 300,- opgelegd wegens overtreding op 28 november 2008 van artikel 10, tweede lid, in verbinding met artikel 11, tweede lid, van de Tabakswet. De rechtbank verklaart het door Eureka ingestelde beroep tegen dit besluit gegrond. Echter, de aangevallen uitspraak wordt door het College vernietigd.
7. (...) Anders dan de minister is de rechtbank van oordeel dat de feitelijke activiteiten in dit geval niet doorslaggevend zijn, nu die, zoals onweerspoken door Eureka is gesteld, slechts van tijdelijke aard kunnen zijn.
Het College oordeelt:
8. “Beslissend is of zij, voor zover in dit kader van belang, een inrichting beheerde voor kunst en cultuur. Daarvoor dient te worden gekeken naar alle op dat moment van belang zijnde feiten en omstandigheden en komt geen beslissende betekenis toe aan het eventuele tijdelijke karakter van de toen bestaande activiteiten. Noch in de Tabakswet noch in het Besluit is voorzien in een afzonderlijke regeling voor activiteiten op het gebied van kunst en cultuur die – eventueel – van tijdelijke aard zijn.”
Op Eureka rust de verplichting maatregelen te treffen ter voorkoming van hinder en overlast van roken. Het tijdelijke karakter van de bestaande activiteiten is niet relevant voor de vraag of het een inrichting beheerde voor kunst en cultuur.
8. Het College kan dit oordeel van de rechtbank evenmin volgen.
Zoals volgt uit hetgeen hiervoor onder 4 is overwogen, is voor de beantwoording van de vraag of Eureka ten tijde van de inspecties in november 2008 en februari 2009 verplicht was maatregelen als bedoeld in artikel 10, eerste lid, van de Tabakswet te hebben getroffen, beslissend of zij, voor zover in dit kader van belang, een inrichting beheerde voor kunst en cultuur. Daarvoor dient te worden gekeken naar alle op dat moment van belang zijnde feiten en omstandigheden en komt geen beslissende betekenis toe aan het eventuele tijdelijke karakter van de toen bestaande activiteiten. Noch in de Tabakswet noch in het Besluit is voorzien in een afzonderlijke regeling voor activiteiten op het gebied van kunst en cultuur die – eventueel – van tijdelijke aard zijn.
Ook gelet op het vorenstaande kan de uitspraak van de rechtbank niet in stand blijven en komt deze voor vernietiging in aanmerking.Beslissing
Het College:
- vernietigt de aangevallen uitspraak;
- doende hetgeen de rechtbank zou behoren te doen:
- verklaart het beroep van Eureka ongegrond.
Nederland: Op lidstaatniveau gezondheidsgegevens regelen
Brief Staatssecretaris V&J aan Eerste Kamer, EU-voorstel: Richtlijn bescherming persoonsgegevens bij gebruik door politiële en justitiële autoriteiten (COM(2012) 10) en EU-voorstel Verordening algemeen kader bescherming persoonsgegevens (COM(2012)11), Kamerstukken I, 2012/13, 33 169, nr. I.
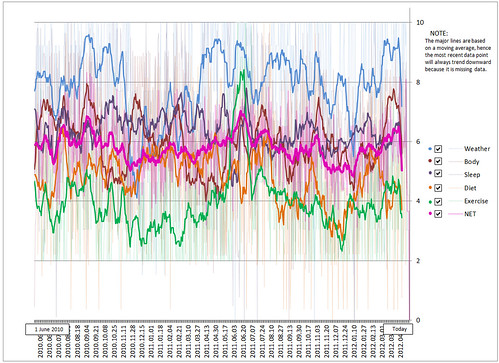 Het voorzitterschap stelt hoofdstuk IX (bijzondere bepalingen met betrekking tot bijzondere gegevensverwerkingen) aan de orde.
Het voorzitterschap stelt hoofdstuk IX (bijzondere bepalingen met betrekking tot bijzondere gegevensverwerkingen) aan de orde.
Bij artikel 81 dat betrekking heeft op de verwerking van gegevens betreffende de gezondheid is Nederland sterk voorstander van de verplichting op lidstaatniveau eigen regel betreffende de verwerking van gegevens betreffende de gezondheid te verwerken. De reikwijdte van de bevoegdheid is echter te beperkt. Maatschappelijk volstrekt aanvaardbare beperkingen van de bescherming van persoonsgegevens ten behoeve van andere verzekeringen dan alleen ziektekostenverzekeringen zijn hard nodig. De vraag is ook of alle overige verwerkingen van gegevens betreffende de gezondheid van publiekrechtelijke en privaatrechtelijke aard wel afdoende zijn afgedekt door deze bepaling.
Artikel 81 betreft de verwerking van gegevens betreffende de gezondheid. Nederland heeft al eerder naar voren gebracht dat de verwerking van gegevens betreffende de gezondheid ook een aanvaardbare toepassing kent bij de uitvoering van andere verzekeringsovereenkomsten dan de ziektekostenverzekering. De Nederlandse tekst van artikel 81 geeft te veel onduidelijkheid over de vraag of, en zo ja, in hoeverre de sociale verzekeringswetgeving ook als algemene grondslag dient voor de verwerking van gezondheidsgegevens. En er zijn tal van andere terreinen waarop gezondheidsgegevens worden verwerkt in een context die maatschappelijk volstrekt aanvaardbaar is. Denk aan het onderwijs en jeugdzorg, het gevangeniswezen, maar ook een sportclub of een werkgever bij een aanstellingskeuring.
Declaraties laboratoriumonderzoeken onverschuldigd betaald
Rechtbank Midden-Nederland 1 mei 2013, LJNBZ9507 (Zilveren Kruis Achmea Zorgverzekeringen N.V. tegen stichting x)
 In 't kort: Kosten laboratoriumonderzoeken. Onverschuldigde betaling. Stichting X is een zelfstandig behandelcentrum en gedaagden vormen samen het bestuur van deze stichting. Verder is gedaagde 1 indirect enig aandeelhouder en bestuurder van bedrijf Y, welke laboratoriumonderzoeken verricht in het kader van geneeskundige zorg en de verkoop van voedingssupplementen. Achmea vordert veroordeling van gedaagde c.s. tot terugbetaling van declaraties betrekking hebbend op in de periode 2007-2010 verrichte laboratoriumonderzoeken.
In 't kort: Kosten laboratoriumonderzoeken. Onverschuldigde betaling. Stichting X is een zelfstandig behandelcentrum en gedaagden vormen samen het bestuur van deze stichting. Verder is gedaagde 1 indirect enig aandeelhouder en bestuurder van bedrijf Y, welke laboratoriumonderzoeken verricht in het kader van geneeskundige zorg en de verkoop van voedingssupplementen. Achmea vordert veroordeling van gedaagde c.s. tot terugbetaling van declaraties betrekking hebbend op in de periode 2007-2010 verrichte laboratoriumonderzoeken.
De rechtbank concludeert dat de declaraties voor de in het geding zijnde laboratoriumonderzoeken onverschuldigd zijn betaald aan stichting X (zorgaanbieder), waarop verzekerden krachtens de polisvoorwaarden geen aanspraak hebben. De rechtbank verwijst de zaak naar de rol voor het nemen een akte door stichting X en houdt iedere verdere beslissing aan.
6.10. De conclusie van het voorgaande is dat de declaraties voor de in het geding zijnde laboratoriumonderzoeken (de onderzoeken aangevraagd door overige eerstelijns zorgverleners) onverschuldigd aan [stichting] zijn betaald. Immers, aan de door Achmea gedane betalingen ligt geen overeenkomst ten grondslag. Noch de overeenkomsten 2007-2010, noch de brief van 27 september 2007 geven [stichting] het recht om ten behoeve van verzekerden van Achmea laboratoriumonderzoeken op aanvraag van overige eerstelijns zorgverleners te verrichten en de kosten daarvan bij Achmea te declareren.
6.11. Nu ingeval van onverschuldigde betaling geen sprake kan zijn van een plicht tot schadebeperking of eigen schuld aan de zijde van Achmea en ook artikel 6:89 BW (klachtplicht) geen toepassing kan vinden, behoeven de in dat verband aangevoerde stellingen geen bespreking. Ten slotte verwerpt de rechtbank het standpunt van [stichting] dat het naar maatstaven van redelijkheid en de billijkheid onaanvaardbaar is wanneer zij de kosten van de verleende zorg terug zou moeten betalen. De in dit verband door [stichting] aangevoerde omstandigheden (zij heeft geen winstoogmerk en kan de omzet van meerdere jaren niet ineens terugbetalen, haar primaire drijfveer is een betere gezondheid tegen lage kosten en alle gedeclareerde zorg is ook daadwerkelijk verleend) zijn onvoldoende om deze conclusie te rechtvaardigen.
6.12. Nu het als onverschuldigd betaald gevorderde bedrag een schatting betreft en door [stichting] wordt betwist, zal de rechtbank Achmea opdragen te bewijzen dat [stichting] voor een bedrag van € 1.375.595,58 declaraties heeft ingediend waaraan geen aanvraag van een bevoegd verwijzer ten grondslag lag. Omdat [stichting] over de aanvragen beschikt en Achmea voornoemd bewijs alleen kan leveren met behulp van die aanvragen, zal [stichting] op grond van artikel 22 Rv worden bevolen om alle aanvragen over de periode 2007-2010 van laboratoriumonderzoeken, verricht buiten de DBC-systematiek, in het geding te brengen.
Voorwaardelijke boete geneesmiddelen zonder vergunning
Strafkamer Rechtbank Amsterdam 3 mei 2013, LJN BZ9379 (voorwaardelijke boete geneesmiddelen) Strafrecht. Geen handelsvergunning. De rechtbank acht bewezen dat er sprake is van voortgezette handeling van medeplegen van poging tot moord, medeplegen van voorbereiding van moord (...) overtreding van een voorschrift, gesteld bij artikel 40 van de Geneesmiddelenwet (meermalen gepleegd) en medeplegen van oplichting. De rechtbank acht verdachte hiervoor strafbaar en veroordeelt verdachte tot een gevangenisstraf van acht jaar, voor wat betreft het in voorraad hebben van de geneesmiddelen een wordt een voorwaardelijke boete gegeven die niet ten uitvoer zal worden gelegd.
Strafrecht. Geen handelsvergunning. De rechtbank acht bewezen dat er sprake is van voortgezette handeling van medeplegen van poging tot moord, medeplegen van voorbereiding van moord (...) overtreding van een voorschrift, gesteld bij artikel 40 van de Geneesmiddelenwet (meermalen gepleegd) en medeplegen van oplichting. De rechtbank acht verdachte hiervoor strafbaar en veroordeelt verdachte tot een gevangenisstraf van acht jaar, voor wat betreft het in voorraad hebben van de geneesmiddelen een wordt een voorwaardelijke boete gegeven die niet ten uitvoer zal worden gelegd.
9.1 Het standpunt van het Openbaar Ministerie
Het Openbaar Ministerie acht bewezen het ten laste gelegde in voorraad hebben en verkopen en/of afleveren en/of ter hand stellen van de in de tenlastelegging genoemde geneesmiddelen waarvoor geen handelsvergunning geldt.
9.2 Het standpunt van de verdediging
De verdediging heeft zich op het standpunt gesteld dat de rechtbank de feiten gelijk aan het requisitoir bewezen kan achten onder de volgende omstandigheden. Verdachte gebruikte de geneesmiddelen met name voor zichzelf en stelde de geneesmiddelen ook nog wel eens aan anderen ter beschikking. Verdachte kende het verboden karakter hiervan niet. Daarbij dient in ieder geval te worden vastgesteld dat verdachte geen professionele handelaar in anabolen is geweest en dat hij zulks evenmin, indien dat wel het geval zou zijn geweest, heeft willen verhullen.
9.3.2 De bewijsoverwegingen
Ten aanzien van het bestanddeel 'geen handelsvergunning' overweegt de rechtbank dat uit het dossier niet is gebleken dat verdachte een handelsvergunning had, op basis waarvan verdachte de geneesmiddelen in voorraad mocht hebben, mocht verkopen, afleveren en/of ter hand stellen.
Hoewel de in de onder 2 ten laste gelegde genoemde middelen niet letterlijk zijn genoemd in de getapte telefoongesprekken en sms'en, is wel af te leiden dat verdachte deze middelen aan anderen heeft verkocht, afgeleverd of ter hand gesteld. Hiervoor is van belang dat uit het NFI-rapport van 15 maart 2012 blijkt dat de in de woning van verdachte aangetroffen en in beslag genomen middelen anabole steroïden zijn. Verdachte heeft verklaard dat anabolen bij hem werden besteld. Daarnaast heeft hij verklaard dat hij de in zijn woning aangetroffen middelen voor zichzelf gebruikte en dat als hij de middelen ging halen ook wel eens voor andere personen meenam. Hieruit volgt dat de middelen die verdachte verkocht, afleverde of ter hand stelde middelen zijn die in de tenlastelegging zijn genoemd.
Dat verdachte het verboden karakter niet kende van het bezit of gebruik, of het zonder winst te maken verkopen, afleveren of ter hand stellen van de genoemde middelen, doet aan een bewezenverklaring niet af. Immers, verdachte wordt niet de opzet hiervan verweten.
14 (...)
Tot slot heeft verdachte de wet op de Economische delicten en de Geneesmiddelenwet overtreden. Nu het hier gaat om feiten die van een geheel andere orde zijn dan die hierboven zijn besproken, en verdachte niet eerder voor soortgelijke feiten is veroordeeld, zal de rechtbank zich ter zake beperken tot het opleggen van een geheel voorwaardelijke geldboete.
17. Beslissing
Veroordeelt verdachte voorts ten aanzien van de overtredingen, zoals bewezen verklaard in zaak B onder 1 en 2 tot een geldboete van € 500,- (zegge: vijfhonderd euro), bij gebreke van betaling en verhaal te vervangen door hechtenis van tien dagen.
Beveelt dat deze geldboete niet zal worden ten uitvoer gelegd, tenzij later anders wordt gelast.
Royalty´s zijn inkomsten uit werkzaamheid, ook wanneer later genoten
Conclusie PG HR 2 april 2013, LJN BZ9161 (X tegen Staatssecretaris van Financiën) en LJN BZ9195
 Als randvermelding. Fiscaal. Belastingen. Royalty vergoeding uit octrooien. Deel van de cassatie slaagt. Belanghebbende heeft in de jaren 1990 t/m 1992 onderzoek verricht aan A in Engeland en was in die jaren niet in Nederland woonachtig. Met A heeft belanghebbende een overeenkomst gesloten op grond waarvan patenten die het resultaat waren van zijn verrichte onderzoeksactiviteiten (medical research / clinical trials), aan A toekwamen. In die overeenkomst is tevens opgenomen dat aan belanghebbende een beloning kon toekomen voortvloeiend uit de commerciële uitbating van die patenten door A. In 2001 en 2005 is aan belanghebbende in verband met die uitbating door A een bedrag aan royalty's toegekend en uitbetaald. De inspecteur heeft voormelde royalty's tot belanghebbendes inkomen uit werk en woning gerekend. Belanghebbende betrekt het standpunt dat het bedrag niet belast is als inkomen uit werk en woning vanwege het ontbreken van een bron van inkomen. Voorts heeft belanghebbende aangevoerd dat de inkomsten toegerekend moeten worden aan een vast middelpunt in Engeland en dat daarom artikel 12, lid 3, van het belastingverdrag moet worden toegepast.
Als randvermelding. Fiscaal. Belastingen. Royalty vergoeding uit octrooien. Deel van de cassatie slaagt. Belanghebbende heeft in de jaren 1990 t/m 1992 onderzoek verricht aan A in Engeland en was in die jaren niet in Nederland woonachtig. Met A heeft belanghebbende een overeenkomst gesloten op grond waarvan patenten die het resultaat waren van zijn verrichte onderzoeksactiviteiten (medical research / clinical trials), aan A toekwamen. In die overeenkomst is tevens opgenomen dat aan belanghebbende een beloning kon toekomen voortvloeiend uit de commerciële uitbating van die patenten door A. In 2001 en 2005 is aan belanghebbende in verband met die uitbating door A een bedrag aan royalty's toegekend en uitbetaald. De inspecteur heeft voormelde royalty's tot belanghebbendes inkomen uit werk en woning gerekend. Belanghebbende betrekt het standpunt dat het bedrag niet belast is als inkomen uit werk en woning vanwege het ontbreken van een bron van inkomen. Voorts heeft belanghebbende aangevoerd dat de inkomsten toegerekend moeten worden aan een vast middelpunt in Engeland en dat daarom artikel 12, lid 3, van het belastingverdrag moet worden toegepast.
De A-G meent dat de criteria 'voordeel beogen en verwachten' geen zelfstandige betekenis hebben indien het voordeel niet in de persoonlijke sfeer ligt maar er wordt deelgenomen aan het economisch verkeer. Nu belanghebbendes activiteiten tweeledig waren en er dus ook in het economisch verkeer werd gehandeld en een voordeel werd behaald, zijn die criteria niet van belang voor de vraag of er een bron van inkomen is. Belanghebbendes primaire standpunt kan hierom niet tot cassatie leiden.
De A-G meent voorts dat belanghebbende in de jaren waarin hij werkzaam was voor A en het onderzoek verrichtte waaruit later de in geschil zijnde inkomsten voortvloeiden, beschikte over een vast middelpunt en dat dat recht deel uitmaakt van het vermogen van de desbetreffende werkzaamheid. Inkomsten daaruit dienen verdragsrechtelijk, ook wanneer zij later worden genoten, daaraan te worden toegerekend. Derhalve geeft het oordeel van het Hof blijk van een onjuiste rechtsopvatting. De hiertegen gerichte klacht van belanghebbende slaagt, aldus de A-G.
Prejudiciële vragen: Zijn onbevruchte menselijke eicellen een menselijke embryo?
UK High Court of Justice, 17 April 2013, [2013] EWHC 807 (Ch), (International Stem Cell Corporation v Comptroller General of Patents)
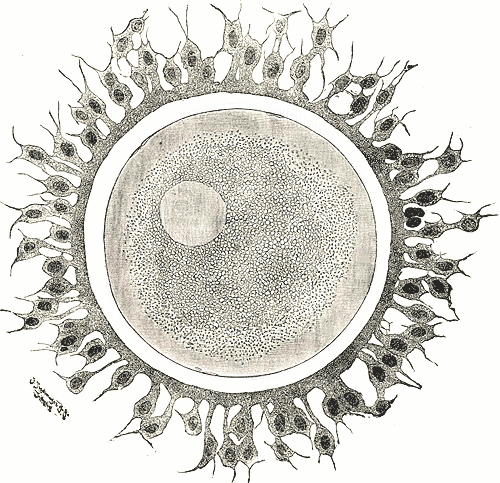 Octrooirecht. Biotechnologische uitvinding. Er wordt voortgebouwd op de Brüstle-vragen/beslissing [LS&R 403]. The question to be referred: The parties have suggested that the following question should be referred. In my judgment this succinctly identifies the issue. Subject to any further submissions, this is the question that I intend to refer:
Octrooirecht. Biotechnologische uitvinding. Er wordt voortgebouwd op de Brüstle-vragen/beslissing [LS&R 403]. The question to be referred: The parties have suggested that the following question should be referred. In my judgment this succinctly identifies the issue. Subject to any further submissions, this is the question that I intend to refer:
Are unfertilised human ova whose division and further development have been stimulated by parthenogenesis, and which, in contrast to fertilised ova, contain only pluripotent cells and are incapable of developing into human beings, included in the term "human embryos" in Article 6(2)(c) of Directive 98/44/EC on the legal protection of biotechnological inventions?
48. As to the referring Judgment, the Comptroller points out that the citation from [44] relied on by ISCC is incomplete. Once one takes into account the remainder of this paragraph, it is much more difficult to suggest that the conclusion of the CJEU expressly contradicted the findings of the Bundesgerichtshof. In particular, the German Court went on to say:
"Independent of this one point in favour of qualification as an embryo as defined in Art. 6 para 2c) of the Directive could be the fact that such cells in any event in the first division stages go through the same development as a fertilized egg cell and therefore appear equally worthy of protection."
My understanding of this passage is that the Bundesgerichtshof was pointing to the similarity between initial stages of development of parthenotes and fertilised egg cells and hypothesising that it could be said that parthenotes were equally worthy of protection from patentability.
49. The Comptroller further submits, correctly in my view, that whilst the Advocate General was clear that the dividing line was whether the cells were totipotent or pluripotent, it does not appear that the CJEU followed this distinction. Unlike the Advocate General, the Court did not frame its decision in relation to parthenotes on a conditional basis, even though it clearly had in mind the distinction between pluripotent and totipotent cells (see paragraph [22] of the CJEU Judgment).
50. Therefore, the Comptroller submits that it is unclear whether the test that the CJEU had in mind turned on merely commencing the process of development of a human being (whether or not the potential exists for the completion of the process), or commencing a process which is capable of leading to the birth of a viable human being. For the reasons given by Mr Mitcheson on behalf of the Comptroller, I agree.
Europees Octrooibureau herroept het "Brüstle" octrooi
EPO persbericht 11 april 2013.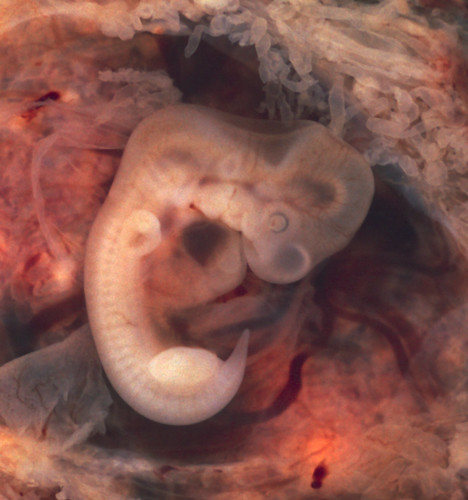 Een bijdrage van Cees Mulder, Maastricht University.
Een bijdrage van Cees Mulder, Maastricht University.
Op 11 april 2013 heeft een oppositieafdeling van het Europees Octrooibureau (EOB) besloten het zogenoemde “Brüstle” octrooi te herroepen tijdens de openbare mondelinge behandeling (Artikel 101(2) EOV).
Het Europees octrooi 1,040,185 getiteld “Neural precursor cells, method for the production and use thereof in neural defect therapy” werd op 22 februari 2006 toegekend aan de Duitse wetenschapper Professor Oliver Brüstle. Het heeft betrekking op en beschrijft het gebruik van neurale voorlopercellen voor medisch toepassingen, met name voor de behandeling van ernstige neurale gebreken zoals Parkinson, Huntington en Alzheimer. Onder andere beschrijft het octrooi hoe de neurale voorlopercellen worden verkregen uit humane embryonale stamcellen. In november 2006 heeft het Amerikaanse bedrijf Geron Corporation oppositie ingesteld tegen verlening van het Europees octrooi, met het verzoek de herroeping van het octrooi. Alle documenten met betrekking tot het octrooi kunnen worden ingezien op het Europees Octrooiregister.
Na bestudering van de argumenten van beide partijen tijdens de oppositieprocedure, heeft de oppositieafdeling besloten het octrooi te herroepen omdat het verleende octrooi meer subject-matter bevat dan de oorspronkelijke ingediende octrooiaanvrage, hetgeen niet is toegestaan volgens Artikel 123 van het Europees Octrooiverdrag (zie ook grond voor oppositie in Artikel 100(c) EOV).
Tegen de beslissing van de oppositieafdeling kan beroep worden ingesteld bij de kamers van beroep (Board of Appeal, Artikel 106 en 108 EOV).
De oppositieafdeling heeft opgemerkt, dat biotechnologische uitvindingen, waaronder die met betrekking tot menselijke embryonale stamcellen, in principe octrooieerbaar zijn onder het Europees Octrooiverdrag (EOV), mits zij nieuw zijn (Artikel 54 EPC) , op uitvinderswerkzaamheid berusten (“inventive step”, Artikel 56 EOV), industrieel toepasbaar zijn (Artikel 57 EOV) en niet uitgezonderd zijn van octrooieerbaarheid onder het EOV (Artikel 53 EOV). Relevant hierbij is de beslissing G 2/06 van de Grote Kamer van Beroep van het EOB (Enlarged Board of Appeal) die aangeeft hoe de uitzonderingen op octrooieerbaarheid onder de EPC inzake stamceltechnologie moeten worden toegepast onder het EOV.
De procedure inzake het Europees octrooi staan los van het parallelle patent dat professor Brüstle in Duitsland heeft verkregen en dat werd gehandhaafd door het Duitse Bundesgerichtshof in november 2012. Hierover is een eerder commentaar op het IE-Forum [IEF 12151] gepubliceerd.
Cees Mulder
Merk RELY-ABLE benadrukt enkel positieve aspecten, dient niet ter onderscheiding
Gerecht EU 30 april 2013, zaak T-640/11 Boehringer Ingelheim International / OHMI (RELY-ABLE) - dossier
 Gemeenschapsmerk. Absolute weigeringsgrond. Vernietiging van beslissing R 756/20114 van de vierde kamer van beroep van het Bureau voor harmonisatie binnen de interne markt (BHIM) van 30 september 2011 houdende verwerping van het beroep tegen de beslissing van de onderzoeker waarbij bescherming als gemeenschapsmerk is geweigerd ten gevolge van een internationale inschrijving voor de Europese Unie van het woordmerk „RELY-ABLE” voor diensten van de klassen 38, 41 en 42 (clinical trial services for pharmaceutical products).
Gemeenschapsmerk. Absolute weigeringsgrond. Vernietiging van beslissing R 756/20114 van de vierde kamer van beroep van het Bureau voor harmonisatie binnen de interne markt (BHIM) van 30 september 2011 houdende verwerping van het beroep tegen de beslissing van de onderzoeker waarbij bescherming als gemeenschapsmerk is geweigerd ten gevolge van een internationale inschrijving voor de Europese Unie van het woordmerk „RELY-ABLE” voor diensten van de klassen 38, 41 en 42 (clinical trial services for pharmaceutical products).
Het beroep wordt verworpen. Het (aangevraagde) merk wordt niet door de consument herinnerd als een merk, maar enkel als een promotioneel woord voor de positieve aspecten van de dienstverlening, namelijk dat men betrouwbaar (reliable) is. Op de Marques-blog.
6. (...) Firstly, the Board of Appeal took the view that the relevant public would directly and unambiguously perceive the sign RELY-ABLE as a deliberate misspelling of the English word ‘reliable’ to make it more ‘catchy’, but would not perceive that spelling as particularly fanciful or arbitrary. Secondly, the Board of Appeal found that the relevant public would directly perceive the message communicated by the sign RELY-ABLE as a whole, as a banal laudatory message relating to an important characteristic of clinical trial services for pharmaceutical products, namely their reliability. (...)
37 Accordingly, the Board of Appeal did not err in dismissing the appeal against the decision refusing protection, after finding, in paragraph 17 of the contested decision, that the word mark RELY-ABLE is not distinctive, on the ground that it could not be perceived and memorised by the relevant consumer as a trade mark, and that the sign as a whole would be perceived as nothing more than a promotional message whose aim is to highlight an important positive aspect of the services, namely that they are reliable.















