HvJ EU 6 februari 2017, IEF 16569; IEFbe 2080; LS&R 1424; C-681/16 (Pfizer tegen Orifarm) ABC. Octrooirecht. Verzoekster is een in IER gevestigde onderneming van het Pfizer-concern. Zij is in het octrooiregister ingeschreven als houdster van een ABC dat is 31-03-2006 afgegeven door het DUI patentbureau voor het in DUI geldende basisoctrooi (voor TNF-bindende eiwitten), in 1989 afgegeven aan AHP Manufacturing en vervallen op 31-08-2010. Het ABC beschermt Etanercept (werkzame stof van het geneesmiddel Enbrel) en geldt als vergunning voor het in de handel brengen. De eerste vergnning voor Enbrel is op 01-02-2000 in ZWI afgegeven en zo geldig voor de EU. Het ABC was in DUI geldig tot 01-02-2015, en na een ‘pediatrische verlenging’ (Vo. 1901/2006) tot 01-09-2015 niet meer geldig. Verweerster (Orifarm in Leverkusen/DUI) maakt deel uit van de DEN Orifarm groep, actief in de parallelimport (uit landen waar de prijzen lager liggen). Zij maakt bij brief van 27-06-2013 aan verzoekster haar voornemen bekend parallelimport te beginnen vanuit EST en LET, en later ook uit andere NLS (BUL, KRO, LIT, POL, ROE, SLW, SLV, TSJ en HON). In april 2015 ontdekt verzoekster op de DUI markt verpakkingen waarop verweerster als parallelimporteur wordt genoemd. Zij start een procedure waarin zij betoogt dat verweerster het ABC heeft geschonden en verzoekt om informatie, terugroeping en vernietiging alsook om vaststelling van de schadevergoedingsplicht. Zij is van mening dat de regelingen van de specifieke mechanismen, die zijn opgenomen in de toetredingsakten van de NLS, op het onderhavige geval van toepassing zijn waardoor verweerster zich niet op het argument van uitputting kon beroepen. Verweerster stelt dat de specifieke mechanismen om verschillende redenen niet van toepassing zijn. (zie de noot van de vertaler onderaan pagina 4 voor wat betreft het verschil in de DUI versie van de toetredingsakten van de begrippen “Besonderen Mechanismus” en “Speziellen Mechanismus”.) Gestelde vragen:
1. Kan degene aan wie een aanvullend beschermingscertificaat is verleend voor de Bondsrepubliek Duitsland zich op de regelingen van de specifieke mechanismen beroepen om te verhinderen dat producten uit de nieuwe lidstaten Tsjechië, Estland, Letland, Litouwen, Hongarije, Polen, Slovenië, Slowakije, Roemenië, Bulgarije en Kroatië (bijlage IV bij de toetredingsakte van 2003, PB 2003, L 236, blz. 797, zoals gewijzigd bij PB 2004, L 126, blz. 4, voor Estland, Letland, Litouwen, Polen, Slovenië, Hongarije, Slowakije en Tsjechië; deel I, bijlage V, punt 1, van de toetredingsakte van 2005, PB 2005, L 157, blz. 268, voor Roemenië en Bulgarije; bijlage IV bij de toetredingsakte van 2011, PB 2012, L 112, blz. 60, voor Kroatië) in de Bondsrepubliek Duitsland worden ingevoerd, wanneer het aanvullende beschermingscertificaat in de Bondsrepubliek Duitsland werd aangevraagd op een tijdstip waarop in die nieuwe lidstaten (die toen nog toetredende landen waren) al regelingen bestonden voor de verkrijging van een dergelijk aanvullend beschermingscertificaat, maar een dergelijk certificaat in die staten niet kon worden aangevraagd door of verleend aan de houder van het voor de Bondsrepubliek Duitsland afgegeven beschermingscertificaat, aangezien deze in de betrokken staten niet beschikte over een basisoctrooi, wat nodig was om een aanvullend beschermingscertificaat te kunnen verkrijgen?




 Octrooirecht. ABC. Directe octrooiinbreuk. Uitleg octrooiconclusie en toegevoegde materie. Het ABC, gebaseerd op
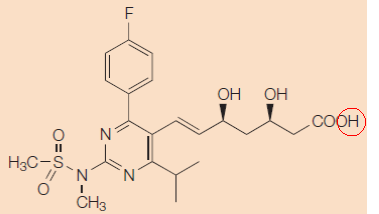
Octrooirecht. ABC. Directe octrooiinbreuk. Uitleg octrooiconclusie en toegevoegde materie. Het ABC, gebaseerd op 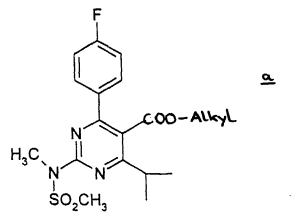 Octrooirecht. ABC. Afstandsleer. Shionogi is farmaceutische onderneming en houdster van ABC 300125 voor 'Rosuvastatinum, desgewenst in de vorm van een niet-toxisch farmaceutisch aanvaardbaar zout, in het bijzonder het calciumzout', voorheen houdster van EP471 'Pyrimidinederivaten als HMG-CoA-reductase-inhibitoren’. Resolution vordert met succes de partiële nietigheid van het octrooi en ABC vanwege toegevoegde materie; voor zover de bescherming ervan zich uitstrekt over andere producten dan in EP 471 genoemde niet-toxische farmaceutisch aanvaardbare zouten van rosuvastatine.
Octrooirecht. ABC. Afstandsleer. Shionogi is farmaceutische onderneming en houdster van ABC 300125 voor 'Rosuvastatinum, desgewenst in de vorm van een niet-toxisch farmaceutisch aanvaardbaar zout, in het bijzonder het calciumzout', voorheen houdster van EP471 'Pyrimidinederivaten als HMG-CoA-reductase-inhibitoren’. Resolution vordert met succes de partiële nietigheid van het octrooi en ABC vanwege toegevoegde materie; voor zover de bescherming ervan zich uitstrekt over andere producten dan in EP 471 genoemde niet-toxische farmaceutisch aanvaardbare zouten van rosuvastatine.














