Uitspraak ingezonden door Marleen van den Horst en Jaap Bremer, BarentsKrans; Julian Eck, Mark van Gardingen en Jan Pot, Brinkhof; Ricardo Dijkstra, Vondst advocaten.
Gelet op bodembeslissingen van ervaren collega octrooi-instanties kan behoorlijk worden getwijfeld over de geldigheid

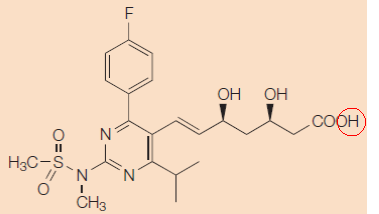
Vzr. Rechtbank Den Haag 5 december 2017, IEF 17330; LS&R 1544; ECLI:NL:RBDHA:2017:14319 (Icos tegen Teva; Sandoz en Mylan). Octrooirecht. Provisionele voorziening. Icos vordert zonder succes provisionele voorziening tot staking van inbreuk op EP 1 173 181 B3 voor de duur van de onderhavige kort gedingen ex 223 Rv. In het VK en Duitsland hebben generieke producenten van tadalafil 'clear the way' procedures gevoerd, het Engelse en Duitse deel van EP 181 zijn nietig bevonden. Gelet op deze bodembeslissingen van ervaren collega octrooi-instanties, alsmede gelet op het feit dat Daugan ook in de onderhavige kort gedingen en in de na te noemen VRO-nietigheidsprocedure ten grondslag is gelegd aan de inventiviteitsaanval, kan ten minste behoorlijk worden getwijfeld over de geldigheid van het Nederlandse deel van het octrooi zodat het opleggen van een provisioneel verbod niet opportuun is. Vorderingen worden afgewezen, aanhouding tot eindvonnis in de meervoudige bodemprocedure tegen TEVA Pharmaceuticals, waarin pleidooi gepland staat op 22 december.